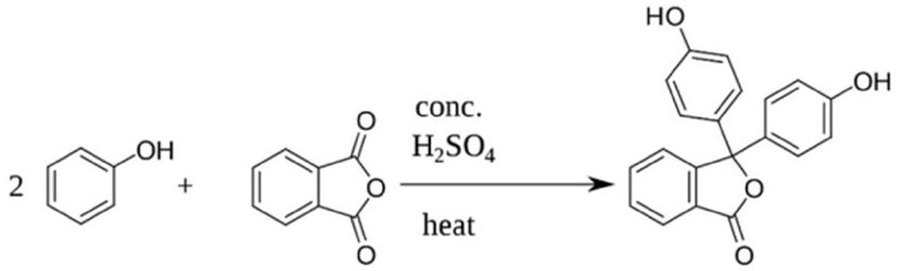
Thuật ngữ acid hoặc base (acid hoặc kiềm) vẫn thường xuất hiện rất phổ biến trong đời sống gia đình. Để nhận biết một dung dịch có môi trường là acid hay là base người ta sử dụng tới chất chỉ thị acid - base. Chất chỉ thị acid - base là chất có màu sắc biến đổi phụ thuộc vào giá trị pH của dung dịch. Một trong những chất chỉ thị thông dụng nhất trong các kĩ thuật chuẩn độ acid - base đó là phenolphthalein. Adolf van Bayer đã phát hiện ra phenolphtalein vào năm 1871. Ông đã quan sát thấy sự hình thành của phenolphtalein khi đun nóng phenol với phthalic anhydride với sự có mặt của acid:
Phenolphthalein là chất rắn kết tinh không màu, đôi khi nó có thể ở dạng bột màu vàng nhạt hoặc màu cam. Đây là một chất không tan trong nước nhưng tan trong cồn. Ở trạng thái tự nhiên, phenolphtalein tồn tại ở dạng acid yếu không màu, được kí hiệu là HIn. Hằng số phân li acid (Ka) của HIn là 3.10-10. Base liên hợp của nó có màu đỏ hồng đậm. Trong dung dịch nước, phenolphthalein sẽ có trạng thái cân bằng như sau:
Theo nguyên lý chuyển dịch cân bằng Le Chatelier, trạng thái cân bằng trên sẽ chuyển dịch sang trái nếu nồng độ của tăng lên, tức là trong dung dịch ưu tiên chiều phản ứng: hơn. Nếu dung dịch có tính base mạnh thì cân bằng chuyển dịch sang phải vì ion OH- sẽ phản ứng với các phân tử Hln chuyển hóa thành In-.
Trong các phép chuẩn độ, phenolphtalein được thêm vào để nhận ra điểm dừng chuẩn độ. Tại điểm này có sự thay đổi màu sắc đột ngột của dung dịch được chuẩn độ vì có sự thay đổi của pH trong môi trường chuẩn độ làm thay đổi trạng thái tồn tại của chất chỉ thị màu, từ đó màu của chỉ thị sẽ thay đổi là một dấu hiệu nhận biết đã đến lúc cần dừng chuẩn độ. Người ta coi rằng có một pH trung gian nào đó một nửa phenolphtalein ở dạng acid và một nửa ở dạng base liên hợp có màu. Độ pH trung gian này có thể được tính theo phương trình Henderson - Hasselbalch cho trạng thái cân bằng chỉ thị:
Trả lời cho các câu 74, 75, 76, 77, 78, 79, 80 dưới đây:
Thuật ngữ acid hoặc base (acid hoặc kiềm) vẫn thường xuất hiện rất phổ biến trong đời sống gia đình. Để nhận biết một dung dịch có môi trường là acid hay là base người ta sử dụng tới chất chỉ thị acid - base. Chất chỉ thị acid - base là chất có màu sắc biến đổi phụ thuộc vào giá trị pH của dung dịch. Một trong những chất chỉ thị thông dụng nhất trong các kĩ thuật chuẩn độ acid - base đó là phenolphthalein. Adolf van Bayer đã phát hiện ra phenolphtalein vào năm 1871. Ông đã quan sát thấy sự hình thành của phenolphtalein khi đun nóng phenol với phthalic anhydride với sự có mặt của acid:

Phenolphthalein là chất rắn kết tinh không màu, đôi khi nó có thể ở dạng bột màu vàng nhạt hoặc màu cam. Đây là một chất không tan trong nước nhưng tan trong cồn. Ở trạng thái tự nhiên, phenolphtalein tồn tại ở dạng acid yếu không màu, được kí hiệu là HIn. Hằng số phân li acid (Ka) của HIn là 3.10-10. Base liên hợp của nó có màu đỏ hồng đậm. Trong dung dịch nước, phenolphthalein sẽ có trạng thái cân bằng như sau:
Theo nguyên lý chuyển dịch cân bằng Le Chatelier, trạng thái cân bằng trên sẽ chuyển dịch sang trái nếu nồng độ của tăng lên, tức là trong dung dịch ưu tiên chiều phản ứng: hơn. Nếu dung dịch có tính base mạnh thì cân bằng chuyển dịch sang phải vì ion OH- sẽ phản ứng với các phân tử Hln chuyển hóa thành In-.
Trong các phép chuẩn độ, phenolphtalein được thêm vào để nhận ra điểm dừng chuẩn độ. Tại điểm này có sự thay đổi màu sắc đột ngột của dung dịch được chuẩn độ vì có sự thay đổi của pH trong môi trường chuẩn độ làm thay đổi trạng thái tồn tại của chất chỉ thị màu, từ đó màu của chỉ thị sẽ thay đổi là một dấu hiệu nhận biết đã đến lúc cần dừng chuẩn độ. Người ta coi rằng có một pH trung gian nào đó một nửa phenolphtalein ở dạng acid và một nửa ở dạng base liên hợp có màu. Độ pH trung gian này có thể được tính theo phương trình Henderson - Hasselbalch cho trạng thái cân bằng chỉ thị:
Trả lời cho các câu 74, 75, 76, 77, 78, 79, 80 dưới đây:
Công thức phân tử của hợp chất phenolphtalein là
A. \({C}_{20}{H}_{14}{O}_{4}\).
B. \({C}_{20}{H}_{16}{O}_{5}\).
C. \({C}_{18}{H}_{14}{O}_{4}\).
D. \({C}_{18}{H}_{16}{O}_{5}\).
Quảng cáo
Trả lời:
Phương pháp giải
Từ CTCT ⟹ CTPT
Giải chi tiết
Công thức phân tử của hợp chất phenolphtalein là \({C}_{20}{H}_{14}{O}_{4}\).
Đáp án cần chọn là: A
Câu hỏi cùng đoạn
Câu 2:
Chọn các đáp án đúng
Thành phần và cấu trúc của phân tử phenolphthalein gồm
A. Vòng thơm 6 cạnh.
B. Phenol.
C. Carboxylic acid no.
D. Aldehyde.
E. Vòng thơm 5 cạnh.
F. Ester.
Phương pháp giải
Từ CTCT ⟹ CTPT
Giải chi tiết
Thành phần và cấu trúc của phân tử phenolphthalein gồm
- Vòng thơm 6 cạnh.
- Phenol.
- Ester.
Đáp án cần chọn là: \(A;B;F\)
Câu 3:
Các nhận định dưới đây là đúng hay sai?
Những yếu tố chỉ ra rằng phenolphthalein là acid yếu là
a. Trong cấu trúc của phenolphthalein có 2 vòng phenol có tính acid yếu nên gây cho phenolphthalein có tính acid yếu.
b. Trong cấu trúc của phenolphthalein có nhóm chức của carboxylic acid nên gây ra tính acid yếu của phenolphthalein.
c. \({K}_{a}\) của acid HIn rất nhỏ, do đó khả năng phân li ra ion \({H}^{+}\)của acid này rất yếu, nên tính acid của HIn yếu.
Phương pháp giải
Phân tích dữ liệu đề bài.
Giải chi tiết
a) đúng. Hai vòng phenol trong cấu trúc có hydro linh động tạo nên tính acid yếu.
b) sai, vì trong cấu trúc của phenolphthalein có nhóm chức của phenol nên gây ra tính acid yếu của phenolphthalein.
c) đúng.
Đáp án cần chọn là: Đ; S; Đ
Câu 4:
Điền số thích hợp vào chỗ trống
pH trung gian mà tại đó người ta mong chờ có sự đổi màu của chỉ thị phenolphtalein là \(\_\_\_\_\) (Làm tròn đến chữ số thập phân thứ nhất)
Đáp án: ____
Đáp án đúng là: 9,5
Phương pháp giải
Người ta coi rằng có một pH trung gian nào đó một nửa phenolphtalein ở dạng acid và một nửa ở dạng base liên hợp có màu. Độ pH trung gian này có thể được tính theo phương trình Henderson - Hasselbalch cho trạng thái cân bằng chỉ thị:
\(pH=pKa+log\frac{\left[ {ln}^{-} \right]}{[HIn]}\)
Giải chi tiết
pH trung gian \(={pK}_{a}=-log\left[ {3.10}^{-10} \right.=9,5\)
Đáp án: 9,5
Đáp án cần điền là: 9,5
Câu 5:
|
không màu |
màu hồng |
HIn |
In- |
Kéo thả các đáp án vào vị trí thích hợp
Khi cho phenolphthalein vào cốc đựng dung dịch nước chanh có \(pH=2,4\) thì chỉ thị __________ . Khi cho phenolphthalein vào cốc đựng dung dịch \(Ba(OH{)}_{2}\) nồng độ 0,1M thì nồng độ ____ của trong dung dịch lớn hơn nồng độ của ____ .
Đáp án đúng là: không màu; In-; HIn
Phương pháp giải
Theo nguyên lý chuyển dịch cân bằng Le Chatelier, trạng thái cân bằng trên sẽ chuyển dịch sang trái nếu nồng độ của \({H}_{3}{O}^{+}\)tăng lên, tức là trong dung dịch ưu tiên chiều phản ứng: \({ln}^{-}+{H}_{3}{O}^{+}→HIn+{H}_{2}O\) hơn. Nếu dung dịch có tính base mạnh thì cân bằng chuyển dịch sang phải vì ion \({OH}^{-}\)sẽ phản ứng với các phân tử Hin chuyển hóa thành \({ln}^{-}\).
Giải chi tiết
Khi cho phenolphthalein vào cốc đựng dung dịch nước chanh có \(pH=2,4\) thì chỉ thị không màu. Khi cho phenolphthalein vào cốc đựng dung dịch Ba( OH\({)}_{2}\) nồng độ 0,1M thì nồng độ của \({ln}^{-}\)trong dung dịch lớn hơn nồng độ của Hin.
Đáp án cần chọn là: không màu ; In- ; HIn
Câu 6:
Để tổng hợp 18 mol phenolphtalein theo quá trình đã được Adolf van Bayer đã phát hiện ra vào năm 1871 cần bao nhiêu gam chất phản ứng? Biết phản ứng có hiệu suất \(90\%\)
A. 6720 gam.
B. 4830 gam.
C. 4820 gam.
D. 3840 gam.
Phương pháp giải
Tính theo PTHH.
Giải chi tiết
\({n}_{Phenol}=2{n}_{phenolphthalein}=36\) (mol)
\({n}_{phthalic anhydride}={n}_{phenolphthalein}=18(mol)\)\(⟹m=(36.94+18.148)/0,9=6720(\) gam \()\)
Đáp án cần chọn là: A
Câu 7:
Nhận định dưới đây là đúng hay sai?
Nồng độ ion \({H}^{+}\)ảnh hưởng tới trạng thái tồn tại của Hin
A. Đúng.
B. Sai.
Phương pháp giải
Theo nguyên lý chuyển dịch cân bằng Le Chatelier, trạng thái cân bằng trên sẽ chuyển dịch sang trái nếu nồng độ của \({H}_{3}{O}^{+}\)tăng lên, tức là trong dung dịch ưu tiên chiều phản ứng: \({ln}^{-}+{H}_{3}{O}^{+}→HIn+{H}_{2}O\) hơn
Giải chi tiết
Nhận định đúng, vì khi tăng nồng độ \({H}^{+}\)cân bằng \(HIn+{H}_{2}O⇌{In}^{-}+{H}_{3}{O}^{+}\)sẽ chuyển dịch sang sang trái, và ngược lại.
Đáp án cần chọn là: \(A\)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 2
Lời giải
1.Đúng vì luôn nghịch biến tức là báo đen có tốc độ giảm dần
nên tốc độ ngựa vằn tăng.
2.Sai. Quãng đường của báo đen đi là:
\({x_1} = \smallint {v_1}\left( t \right)dt = \smallint 15 \cdot {e^{ - 0,1t}}dt = - 150{e^{ - 0,1t}} + {C_1}\)\({x_1}\left( 0 \right) = - 150{e^0} + {C_1} = 0 \Leftrightarrow {C_1} = 150 \Rightarrow {x_1} = - 150{e^{ - 0,1t}} + 150\)Tương tự quãng đường của ngựa vằn đi là:
\({x_2}\left( t \right) = \smallint {v_2}\left( t \right)dt = \smallint \left( {20 - 20{e^{ - 0,1t}}} \right)dt = 20t + 200{e^{ - 0,1t}} + {C_2}\)\({x_2}\left( 0 \right) = 20.0 + 200.{e^0} + {C_2} = 40 \Leftrightarrow {C_2} = 40 - 200 = - 160\)\( \Rightarrow {x_2}\left( t \right) = 20t + 200{e^{ - 0,1t}} - 160\)Khoảng cách báo đen và ngựa vằn là
\({\rm{\Delta }}x = {x_2} - {x_1} = 20t + 200{e^{ - 0,1t}} - 160 + 150{e^{ - 0,1t}} - 150 = 20t + 250{e^{ - 0,1t}} - 310 = f\left( t \right)\)Xét \(f'\left( t \right) = 20 - 35{e^{ - 0,1t}} = 0 \Leftrightarrow {e^{ - 0,1t}} = \frac{{20}}{{35}} \Leftrightarrow t = - 10{\rm{ln}}\left( {\frac{{20}}{{35}}} \right)\)
Khi đó \({\rm{min}}f\left( t \right) = f\left( { - 10{\rm{ln}}\frac{{20}}{{35}}} \right) \approx 1,92315\)
Khoảng cách min này đạt được khi điều này là sai
Vậy 2,3 sai.
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Khi đánh bắt cá tại một quần thể ở ba thời điểm, thu được tỉ lệ như sau:
| I | II | III | |
|
Trước sinh sản
|
\(55\%\)
|
\(42\%\)
|
\(20\%\)
|
|
Đang sinh sản
|
\(30\%\)
|
\(43\%\)
|
\(45\%\)
|
|
Sau sinh sản
|
\(15\%\)
|
\(15\%\)
|
\(35\%\)
|
Có bao nhiêu nhận xét đúng trong các nhận xét sau:
1. Tại thời điểm I quần thể đang ở trạng thái phát triển
2. Tại thời điểm II có thể tiếp tục đánh bắt với mức độ vừa phải
3. Tại thời điểm I có thể tiếp tục đánh bắt
4. Tại thời điểm III quần thể đang bị đánh bắt quá mức nên cần được bảo vệ
5. Tại thời điểm III có thể tiếp tục đánh bắt
A. 1.
B. 4.
C. 3.
D. 2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.