Biodiesel là hỗn hợp methyl ester của acid béo (RCOOCH3), được tạo thành khi chất béo phản ứng với methanol dư trong môi trường kiềm. Từ 200 kg dầu ăn đã qua sử dụng (chứa 80% chất béo về khối lượng, còn lại là tạp chất không tạo biodiesel) sản xuất được tối đa m (kg) biodiesel. Biết: phân tử khối trung bình của chất béo là 880 amu, hiệu suất quá trình sản xuất đạt 90%. Giá trị của m là bao nhiêu? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng đơn vị).
Quảng cáo
Trả lời:
Đáp án:
Đáp án: 145
(RCOO)3C3H5 + 3CH3OH → 3RCOOCH3 + C3H5(OH)3
M chất béo = 3R + 173 = 880 → R = 707/3
m = 200.80%.90%.3(R + 59)/880 = 145 kg
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Đáp án:
Đáp án: 0,97
C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(g) (1)
C8H18(l) + 12,5O2(g) → 8CO2(g) + 9H2O(g) (2)
Δr\({H}_{298}^{0}\) (1) = -393,5.2 – 241,8.3 – (-277,6) = -1234,8 kJ
Δr\({H}_{298}^{0}\) (2) = -393,5.8 – 241,8.9 – (-249,9) = -5074,3 kJ
Đốt 1L xăng E10 (100 mL C2H5OH + 900 mL C8H18) tỏa ra nhiệt lượng:
Q1 = 1234,8.100.0,789/46 + 5074,3.900.0,703/114 = 30280,315 kJ
Đốt 1L xăng truyền thống (1000 mL C8H18) tỏa ra nhiệt lượng:
Q2 = 5074,3.1000.0,703/114 = 31291,517 kJ
→ k = Q1/Q2 ≈ 0,97
Câu 2
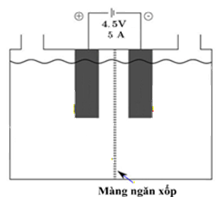
Phần dung dịch bên phía anode chuyển sang màu xanh chứng tỏ có I2 sinh ra và nhận định của nhóm học sinh trên là đúng.
Nếu cho phenolphthalein vào phần dung dịch bên phía cathode, dung dịch sẽ chuyển thành màu hồng.
Sau khi điện phân, nếu tháo màng ngăn, khuấy đều dung dịch sẽ tạo thành nước Javel.
Sau điện phân, nhóm học sinh trên lấy 5 mL dung dịch bên anode đem pha loãng bằng nước cất và chuẩn độ bằng dung dịch Na2S2O3 0,1 M đến khi dung dịch mất màu thì dùng hết 29,8 mL. Biết phương trình chuẩn độ: 2Na2S2O3 + I2 → Na2S4O6 + 2NaI. Nồng độ mol/L của I2 được xác định bằng phương pháp chuẩn độ trên là 0,298M. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần nghìn).
Lời giải
a) Sai, tại anode có Cl-, I-, H2O.
E°Cl2/2Cl- > E°I2/2I- chứng tỏ I- có tính khử mạnh hơn Cl- và I- trực tiếp bị oxi hóa tại anode thành I2, do đó nhận định trên là không đúng.
Chú ý: Ban đầu Cl- và I- cùng nồng độ, rõ ràng I- mạnh mẽ hơn và chiếm suất điện phân trước. Tới lúc nào đó nồng độ I- giảm dần, Cl- nhờ ưu thế nồng độ sẽ bắt đầu bị điện phân. Vì vậy Cl2 oxi hóa I- là có xảy ra, nhận định sai vì khẳng định “chỉ có ion Cl- bị oxi hóa”.
b) Đúng, tại cathode xuất hiện OH- làm phenolphthalein chuyển sang màu hồng:
2H2O + 2e → 2OH- + H2
c) Sai, với bình điện phân như vậy thì Cl2 (nếu có, xuất hiện sau khi I- đã giảm tới mức nào đó) cũng đã thoát ra ngoài nên kết thúc điện phân mới tháo màng ngăn thì không còn đủ Cl2 để tạo nước Javel nữa.
d) Đúng:
nNa2S2O3 = 2,98 mmol → nI2 = 1,49 mmol
→ CM I2 = 1,49/5 = 0,298M
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
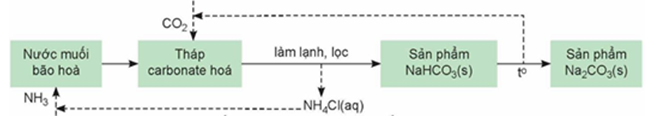
Phản ứng tổng hợp NH3 là phản ứng thuận nghịch và phản ứng theo chiều thuận là tỏa nhiệt.
Việc tăng áp suất làm tăng hiệu suất tạo NH3.
Sau một quy trình, hiệu suất chuyển hóa N2 là 60%.
Việc tuần hoàn khí chưa phản ứng giúp tiết kiệm nguyên liệu quá trình sản xuất.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Ở Bước 1, có thể thay thế 2mL dầu thải bằng 2 gam mỡ lợn.
Sau Bước 3, lọc lấy chất rắn, phần dung dịch còn lại cho phản ứng với Cu(OH)2 thấy tạo thành dung dịch màu xanh lam.
Xà phòng khi hòa tan trong nước tạo ra dung dịch có môi trường acid.
Kết quả của thí nghiệm phù hợp với giả thuyết của nhóm học sinh.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.