Em hãy dự đoán trong các phản ứng sau, phản ứng nào có ∆S > 0, ∆S < 0 và ∆S ≈ 0. Giải thích.
a) C(s) + CO2(g) → 2CO(g)
b) CO(g) + O2(g) → CO2(g)
c) H2(g) + Cl2(g) → 2HCl(g)
d) S(s) + O2(g) → SO2(g)
e) Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Em hãy dự đoán trong các phản ứng sau, phản ứng nào có ∆S > 0, ∆S < 0 và ∆S ≈ 0. Giải thích.
a) C(s) + CO2(g) → 2CO(g)
b) CO(g) + O2(g) → CO2(g)
c) H2(g) + Cl2(g) → 2HCl(g)
d) S(s) + O2(g) → SO2(g)
e) Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Quảng cáo
Trả lời:
Lưu ý:
- Các phản ứng hóa học làm tăng số mol khí thường có biến thiên entropy dương (∆S > 0).
- Các phản ứng hóa học làm giảm số mol khí thường có biến thiên entropy âm (∆S < 0)
- Các phản ứng hóa học không làm thay đổi số mol khí hoặc phản ứng không có chất khí sẽ có biến thiên entropy nhỏ (∆S ≈ 0)
a) Phản ứng làm tăng số mol khí ⇒ ∆S > 0
b) Phản ứng làm giảm số mol khí ⇒ ∆S < 0
c) Phản ứng có số mol khí trước và sau phản ứng bằng nhau ⇒ ∆S ≈ 0
d) Phản ứng có số mol khí trước và sau phản ứng bằng nhau ⇒ ∆S ≈ 0
e) Phản ứng làm tăng số mol khí ⇒ ∆S > 0
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Hòa tan vôi sống (CaO) vào nước là phản ứng tỏa nhiệt
∆H của phản ứng mang dấu âm hay ∆H < 0.
Lời giải
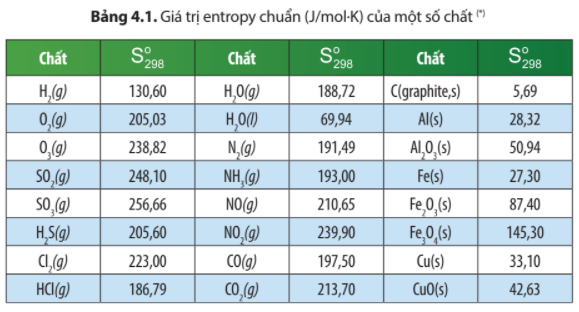
= (CO, g) + × (O2, g) - (CO2, g)
= -110,05 + × 0 – (–393,51) = 283,46 (kJ)
= × (O2, g) + (CO, g) - (CO2, g)
= × 205,03 + (-197,50) - 213,69 = -308,675 J/K
= - 298.
= 283,46.103 – 298. (-308,675) = 375445,15 J > 0
⇒ Phản ứng trên không tự xảy ra.
b) Để phản ứng trên tự xảy ra, cần có:
= - T. < 0
⇔ 283,46.103 – T. (-308,675) < 0
⇔ T > 918 K hay T > 645 oC
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.