Phổ IR của hợp chất hữu cơ X (chỉ chứa C, H, O) và số sóng hấp thụ của một số
loại liên kết được biểu diễn ở hình sau:
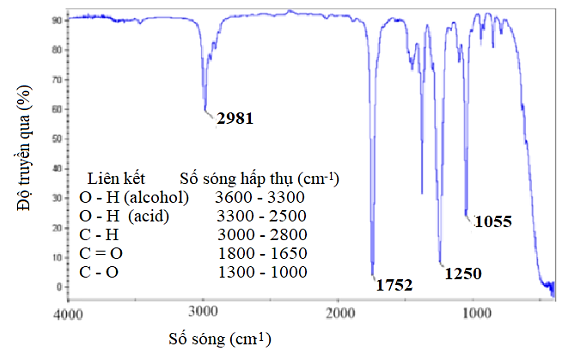
Tín hiệu hồng ngoại của liên kết O - H có đặc điểm là chân rộng và đỉnh tù. Phổ
khối lượng (MS) của hợp chất X có peak ion phân tử ở giá trị m/z = 74.
Cho 0,1 mol chất X tác dụng với 175 mL dung dịch NaOH 1,0 M, cô cạn dung dịch
sau phản ứng thu được a gam chất rắn khan, trong đó có chứa chất hữu cơ Y, biết
Giá trị của a là bao nhiêu (nhập đáp án vào ô trống)?
Quảng cáo
Trả lời:
Đáp án:
X có số sóng hấp thụ ở X có liên kết −C=O.
X có số sóng hấp thụ ở X có liên kết −C−O.
X có số sóng hấp thụ ở (chân hẹp, đỉnh nhọn) X có liên kết C – H X là ester.
Mà phổ MS của hợp chất X có peak ion phân tử ở giá trị m/z = 74
X là
Mà thuỷ phân X thu được hợp chất hữu cơ Y có
X có công thức cấu tạo là:
Vậy Y là:
Có
Áp dụng định luật bảo toàn khối lượng ta có:
Đáp án: 11,2
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
1,06%.
2,12%.
10,6%.
21,2%.
Lời giải
Mẫu X gồm có NaOH (a mol) và (b mol)
* Khi hòa tan hoàn toàn trong HCl xảy ra các phản ứng hóa học sau:
NaOH + HCl → NaCl + (1)
(2)
⇒ Dung dịch Y thu được gồm HCl dư và NaCl.
* Tiến hành chuẩn độ dung dịch Y với NaOH
HCl + NaOH → NaCl + (3)
Ta có:
⇒ phản ứng hết với 100 mL dung dịch Y là: 0,00263.10 = 0,0263 mol
Theo bài, ta có hệ phương trình:
Hàm lượng trong mẫu X là:
Chọn D.
Lời giải
→ 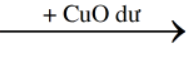
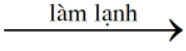 N2.
N2.
Sau khi ngưng tụ còn lại khí N2 ⟹ = 0,3 mol = (ban đầu).
N2 + 3H2 ⇌ 2NH3
3CuO + 2NH3 3Cu + N2 + 3H2O
CuO + H2 Cu + H2O
mchất rắn giảm = mO phản ứng = 12,8 gam ⟹ nO phản ứng = 0,8 mol.
Bảo toàn electron toàn bộ quá trình: (ban đầu) = 2nO phản ứng ⟹ (ban đầu) = 0,8 (mol).
Ta thấy: ⟹ Hiệu suất tính theo H2.
N2 + 3H2 ⇌ 2NH3
Ban đầu: 0,3 0,8 (mol)
Phản ứng: x 3x 2x (mol)
Sau: (0,3 − x) (0,8 − 3x) 2x (mol)
⟹ nSau = (0,3 − x) + (0,8 − 3x) + 2x = 1,1 − 2x (mol)
Mà = 10% ⟹ = 1,1 ⟹ x = 0,05.
Chọn A.
Câu 3
chất khử.
chất oxi hóa.
vừa là chất khử, vừa là chất oxi hóa.
acid.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Giảm áp suất, tăng nhiệt độ, có xúc tác.
Giảm áp suất, giảm nhiệt độ, có xúc tác.
Tăng áp suất, giảm nhiệt độ, có xúc tác.
Tăng áp suất, tăng nhiệt độ, có xúc tác.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A. Na2CO3, H2SO4.
B. CO2, KHSO4.
C. NaHCO3, Na2SO4.
D. CO2, BaSO4.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
(1), (3) và (4).
(1), (2) và (5).
(2), (3) và (4).
(1), (3) và (5).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.