(0,5). Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy hoàn toàn khí methane như sau: CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
(a) Tính biến thiên enthalpy chuẩn () của phản ứng trên và cho biết phản ứng trên là tỏa nhiệt hay thu nhiệt? Giải thích.
(b) Tính thể tích khí methane (ở điều kiện chuẩn) cần dùng để cung cấp 712,4 kJ nhiệt lượng. Giả sử phản ứng xảy ra hoàn toàn và không có sự thất thoát nhiệt lượng.
Cho biết nhiệt tạo thành chuẩn của một số chất
(Nguồn: Silberberg, Martin. (2018). Chemistry: the molecular nature of matter and change with advanced topics. McGraw-Hill Education.)
|
Chất |
CH4(g) |
O2(g) |
CO2(g) |
H2O(l) |
|
(kJ/mol hay kJ mol-1) |
–74,9 |
0 |
–393,5 |
–285,8 |
Câu hỏi trong đề: Bộ 68 đề thi cuối kì 2 Hóa học 10 năm 2023-2024 có đáp án !!
Quảng cáo
Trả lời:
a. CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
Áp dụng công thức ta có:
∆r H0298 = ∆f H0298(CO2(g)) + 2∆f H0298(H2O(l)) - ∆f H0298(CH4(g)) -∆f H0298(O2(g))
∆r H0298 = -393,5 + 2.(-285,8) - (-74,6) - 0 = - 890,5 (kJ).
Phản ứng trên tỏa nhiệt, vì ∆r H0298 < 0.
b. Đốt cháy 1 mol CH4(g) tỏa ra nhiệt lượng 890,5 kJ Đốt cháy x mol CH4(g) tỏa ra nhiệt lượng 712,4 kJ
x = 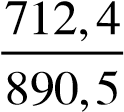 = 0,8 (mol)
= 0,8 (mol)
Thể tích khí methane (ở đkc) cần dùng là: 0,8×24,79 = 19,832 (L).
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
1, 3.
chỉ 3.
1, 2.
1, 2, 3.
Lời giải
Đáp án đúng là A
Lời giải
a. Yếu tố là diện tích tiếp xúc.
b. Yếu tố nồng độ.
c. Yếu tố chất xúc tác.
d. Yếu tố nhiệt độ.
Câu 3
Nồng độ khí O2.
Chất xúc tác.
Kích thước các tinh thể KClO3.
Nhiệt độ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Nhiệt độ.
Áp suất.
Chất xúc tác.
Diện tích tiếp xúc.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Quá trình tự oxi hóa – khử.
Quá trình nhận proton.
Quá trình khử .
Quá trình oxi hóa.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 6
0,2M.
2M.
1M.
0,1M.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















