1. Phenol được phát hiện vào năm 1834, khi nó được chiết xuất từ nhựa than đá. Phần lớn phenol được dùng để sản xuất poli(phenolfomanđehit) (dùng làm chất dẻo, chất kết dính).
Anđehit axetic là chất khí không màu, mùi xốc, tan rất tốt trong nước và các dung môi hữu cơ, chủ yếu được dùng để sản xuất axit axetic.
Từ axetilen, hãy viết phương trình phản ứng điều chế phenol và anđehit axetic theo sơ đồ sau, ghi rõ điều kiện (nếu có):
benzen clobenzen natri phenolat phenol
axetilen etilen anđehit axetic.
2. Phân biệt: anđehit axetic (CH3CHO), axit axetic (CH3COOH), phenol (C6H5OH), etanol (C2H5OH), hexan (C6H14).
Câu hỏi trong đề: Bộ 10 Đề thi Hóa học 11 Học kì 2 có đáp án !!
Quảng cáo
Trả lời:
1.
Axetilen: CHCH; Anđehit axetic: CH3CHO.
Sơ đồ phản ứng:
C6H6C6H5Cl C6H5ONaC6H5OH
C2H2C2H4CH3CHO.
(1) 3CHCH C6H6
(2) C6H6+ Cl2C6H5Cl + HCl
(3) C6H5Cl + NaOH C6H5ONa + NaCl
(4) C6H5ONa + CO2+ H2O C6H5OH + NaHCO3
(5) CHCH + H2CH2=CH2
(6) 2CH2=CH2+ O22CH3CHO
2.
- Trích mẫu thử.
- Dùng quỳ tím cho vào từng mẫu thử:
+ Dung dịch làm quỳ tím hóa đỏ là CH3COOH.
+ Không làm đổi màu quỳ tím: CH3CHO, C6H5OH, C2H5OH, C6H14(nhóm I)
- Dùng dung dịch Br2cho vào từng mẫu thử ở nhóm I.
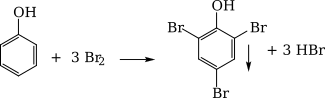
+ Thấy tạo thành kết tủa trắng là C6H5OH.
+ Chỉ thấy dung dịch Br2nhạt màu là CH3CHO.
CH3CHO + Br2+ H2O CH3COOH + 2HBr
+ Không có hiện tượng gì: C2H5OH, C6H14.
Dùng kim loại Na:
+ Thấy có khí thoát ra là C2H5OH.
C2H5OH + Na C2H5ONa + \(\frac{1}{2}\) H2
+ Không có hiện tượng gì là C6H14.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
X gồm: ancol propylic (CH3CH2CH2OH) và phenol (C6H5OH).
Phần I: \({n_{B{r_2}}}\)= 0,15 (mol).
Phương trình hóa học:

nphenol= n=\(\frac{{{n_{B{r_2}}}}}{3}\) = 0,05 (mol).
a = m= 0,05×331 = 16,55 (gam).
Phần II: \({n_{{H_2}}}\)= 0,075 (mol).
Phương trình hóa học;
CH3CH2CH2OH + Na CH3CH2CH2ONa + \(\frac{1}{2}\)H2
C6H5OH + Na C6H5ONa + \(\frac{1}{2}\)H2
\({n_{{C_3}{H_7}OH}} + {n_{{C_6}{H_5}OH}} = 2{n_{{H_2}}} = 0,15\)(mol)
\({n_{{C_3}{H_7}OH}}\) = 0,15 – 0,05 = 0,1 (mol)
m = mX= \({m_{{C_3}{H_7}OH}} + {m_{{C_6}{H_5}OH}}\)= 2×(0,1×60 + 0,05×94) = 21,4 (gam).
Lời giải
X gồm glixerol (C3H5(OH)3) và một ankanol A (CnH2n+2O).
a. Sơ đồ phản ứng: X + O2CO2+ H2O.
\({n_{{O_2}}}\)= 0,975 (mol); \({n_{{H_2}O}}\)= 1 (mol).
\({n_{Cu{{(OH)}_2}}}\)= 0,025 (mol).
\({n_{{C_3}{H_5}{{(OH)}_3}}} = 2{n_{Cu{{(OH)}_2}}}\)= 2×0,025×3 = 0,15 (mol) (do chỉ tác dụng 1/3 hỗn hợp X).
Gọi số mol của ankanol A là x (mol) và số mol CO2sinh ra khi đốt cháy X là y (mol).
Ta có: nX= \({n_{{H_2}O}} - {n_{C{O_2}}}\)
0,15 + x = 1 – y x + y = 0,85 (*).
Bảo toàn nguyên tố O: nO(X)+ 2\({n_{{O_2}}}\)= 2\({n_{C{O_2}}}\)+ \({n_{{H_2}O}}\).
3×0,15 + x + 2×0,975 = 2y + 1
x – 2y = -1,4 (**).
Từ (*) và (**), suy ra: x = 0,1; y = 0,75.
Ta có: \({n_{C{O_2}}}\)= 3×0,15 + 0,1×n = 0,75 n = 3
Ankanol A là C3H8O.
a = mX= 0,15×92 + 0,1×60 = 19,8 (gam).
b. A Y (anđehit + H2O + Ancol dư).
A là ancol bậc I: CH3CH2CH2OH.
CH3CH2CH2OH + CuO CH3CHO + H2O + Cu
nancol(pư)= \({n_{{H_2}O}}\).
nA= nancol(pư) + nancol(dư) = 2\({n_{{H_2}}}\)= \(\frac{{0,448}}{{22,4}}\) = 0,02 (mol).
b = mA= 0,02×60 = 1,2 (gam).
c. \({n_{{C_3}{H_7}OH}} = \frac{3}{{60}} = 0,05\)(mol); \({n_{C{H_3}OH}} = \frac{{1,6}}{{32}} = 0,05\) (mol)
\(\sum {{n_{ancol}}} \)= 0,05 + 0,05 = 0,1 (mol).
Sơ đồ phản ứng: 2ancol Ete + H2O.
\({n_{{H_2}O}} = \frac{{{n_{ancol}}}}{2} = 0,05\)(mol).
Bảo toàn khối lượng:
mancol= mete+ \({m_{{H_2}O}}\)
3 + 1,6 = m+ 0,05×18 m= 3,7 (gam).
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















