Để xác định nồng độ dung dịch NaOH người ta tiến hành như sau: Cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. Lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng.
A. 0,1143M.
B. 0,2600M.
C.0,1240M.
D.0,1600M.
Câu hỏi trong đề: ĐGNL ĐHQG Hà Nội - Khoa học tự nhiên - Chuẩn độ dung dịch !!
Quảng cáo
Trả lời:
Bước 1: Tính n(COOH)2trong 10 ml dung dịch axit oxalic
- \[{n_{{H_2}{C_2}{O_4}.2{H_2}O}} = \frac{{1,26}}{{90 + 18.2}} = 0,01\left( {mol} \right)\]
- 100 ml dung dịch axit oxalic chứa 0,01 mol (COOH)2
10 ml ⟶ 0,001 mol
Bước 2: Tính nNaOH
- Phenolphtalein xuất hiện màu hồng ở pH = 9 >7 ⟹ NaOH dư, (COOH)2hết
- Đặt nNaOH= x mol.
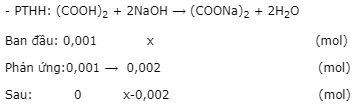
pH = 9 ⟹ pOH = 14 - 9 = 5 ⟹ [OH-]sau pư= 10-5
Bước 3: Tính CM NaOH
- Ta có:\[{\left[ {O{H^ - }} \right]_{sau{\kern 1pt} pu}} = \frac{{x - 0,002}}{{(10 + 17,5){{.10}^{ - 3}}}} = {10^{ - 5}} \Rightarrow {\rm{ }}x{\rm{ }} = {\rm{ }}{2,000275.10^{ - 3}}.\]
\[ \Rightarrow {\rm{ }}{C_{M{\rm{ }}NaOH}}\; = \frac{{{n_{NaOH}}}}{{{V_{dd{\kern 1pt} NaOH}}}} = \frac{{{{2,000275.10}^{ - 3}}}}{{{{17,5.10}^{ - 3}}}} = {\rm{ }}0,1143{\rm{ }}M.\]
Đáp án cần chọn là: A
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Bước 1: Tính số mol của Na2S2O3
nNa2S2O3= 0,018.0,05 = 9.10-4mol
Bước 2: Viết phương trình phản ứng, tính số mol các chất theo PTHH
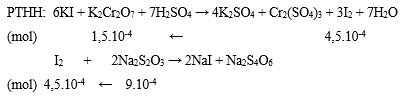
Bước 3: Tính CMcủa K2Cr2O7
⟹ CM K2Cr2O7= 1,5.10-4/0,01 = 0,0015M.
Đáp án cần chọn là: C
Câu 2
A. 68,4%.
B. 9,12%.
C.31,6%.
D.13,68%.
Lời giải
Bước 1: Tính nFe2+ trong 20 ml dd Y
- nKMnO4= 0,1.0,03 = 0,003 mol
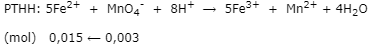
- Trong 20 ml dung dịch Y có 0,015 mol Fe2+
⟹ 150 ml dung dịch Y có x mol nFe2+
⟹ nFe2+ = 0,015.150/20 = 0,1125 mol
Bước 2: Tính %mFeSO4trong X
- mFeSO4= 0,1125.152 = 17,1 gam
→ %mFeSO4= (17,1/25).100% = 68,4%.
Đáp án cần chọn là: A
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A.0,25M.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
A.9%.
B.17%.
C.12%.
D.21%.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















