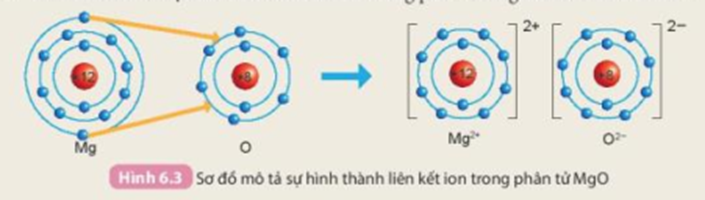
Quan sát Hình 6.2 và so sánh số electron ở lớp ngoài cùng của nguyên tử Na, Cl với ion Na+, Cl-.
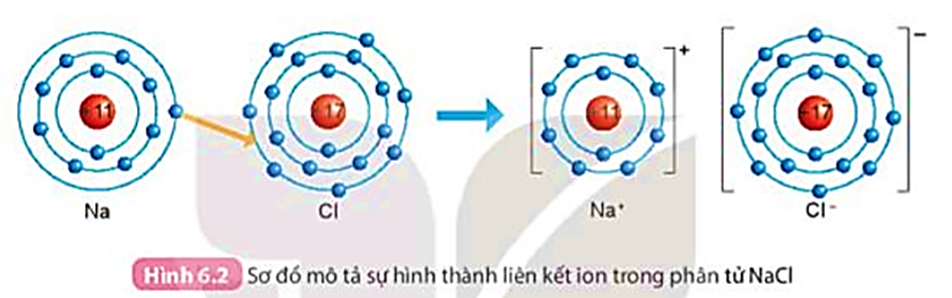
Quan sát Hình 6.2 và so sánh số electron ở lớp ngoài cùng của nguyên tử Na, Cl với ion Na+, Cl-.

Câu hỏi trong đề: Bài tập Giới thiệu về liên kết hóa học có đáp án !!
Quảng cáo
Trả lời:
- Số electron ở lớp ngoài cùng của Na là 1, còn số electron ở lớp ngoài cùng của ion Na+ là 8.
- Số electron ở lớp ngoài cùng của Cl là 7, còn số electron ở lớp ngoài cùng của ion Cl- là 8.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
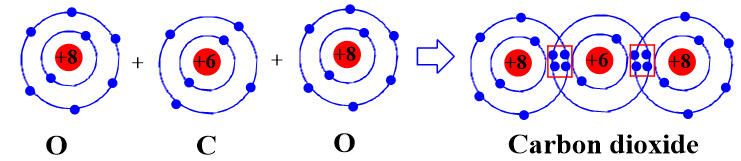
- Sự hình thành liên kết cộng hóa trị trong phân tử carbon dioxide
Khi hình thành phân tử carbon dioxide, hai nguyên tử O đã liên kết với một nguyên tử C bằng cách nguyên tử C đã góp chung với mỗi nguyên tử O hai electron tạo thành 2 cặp electron dùng chung.
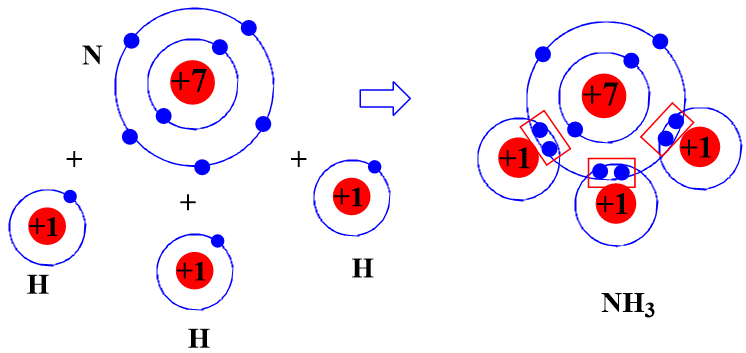
- Sự hình thành liên kết cộng hóa trị trong phân tử ammonia
Khi hình thành phân tử ammonia, ba nguyên tử H đã liên kết với một nguyên tử N bằng cách nguyên tử N đã góp chung với mỗi nguyên tử H một electron tạo thành cặp electron dùng chung.
Lời giải
- Muối ăn là hợp chất ion nên là chất rắn ở điều kiện thường, khó bay hơi, khó nóng chảy.
- Đường ăn và nước đá là hợp chất cộng hóa trị nên ở thể rắn, dễ nóng chảy và nước ở thể lỏng sẽ dễ bay hơi do các chất cộng hóa trị thường có nhiệt độ nóng chảy và nhiệt độ sôi thấp.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.