Methane cháy tỏa nhiệt lớn nên được dùng làm nhiên liệu. Khi trộn methane và oxygen với tỉ lệ thích hợp thì sẽ tạo ra hỗn hợp nổ.
Biến thiên enthalpy của phản ứng trên được tính toán dựa trên các giá trị nào?
Quảng cáo
Trả lời:
CH4(g) + 2O2(g) CO2(g) + 2H2O(l)
Biến thiên enthalpy của phản ứng cháy của methane có thể được tính theo hai cách:
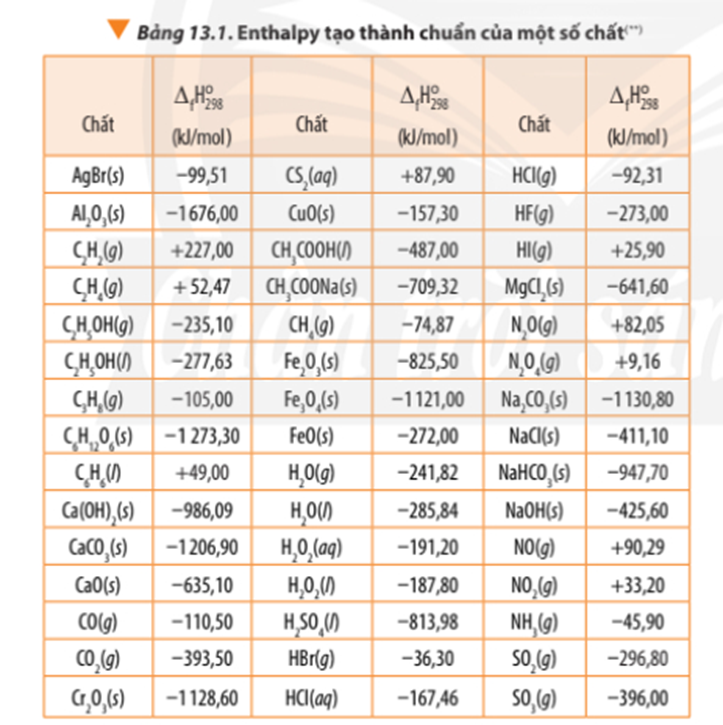
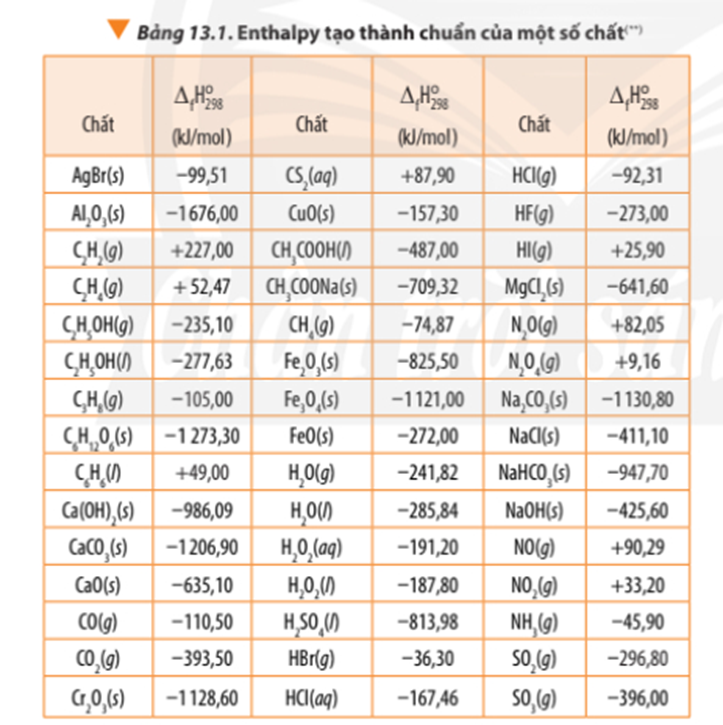
- Cách 1: Dựa vào nhiệt tạo thành chuẩn của các chất.
∆r = ∆f(CO2) + 2.∆f(H2O) – ∆f(CH4) – 2.∆f(O2)
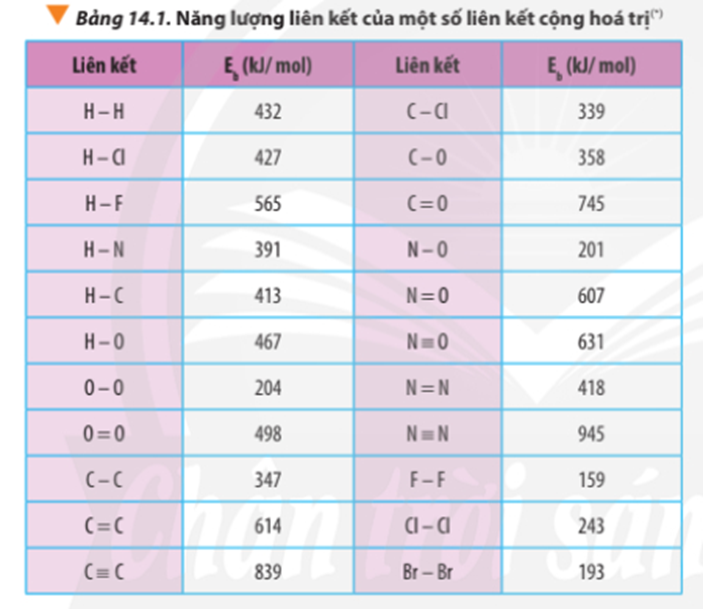
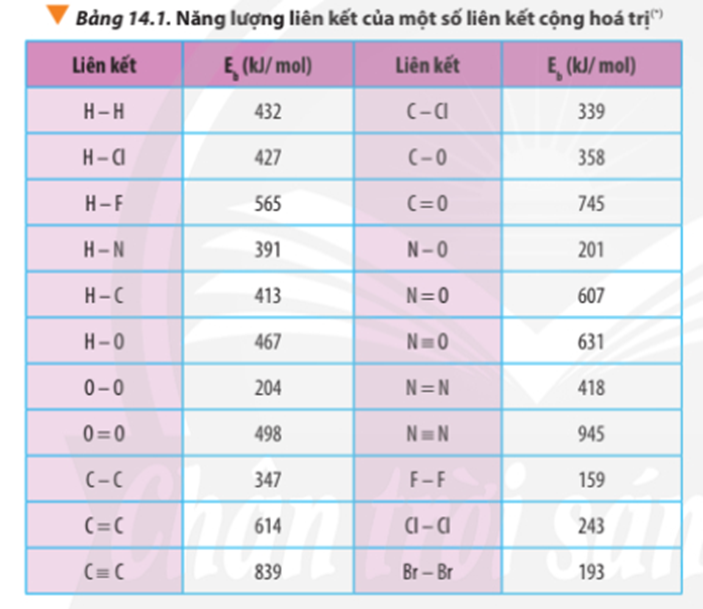
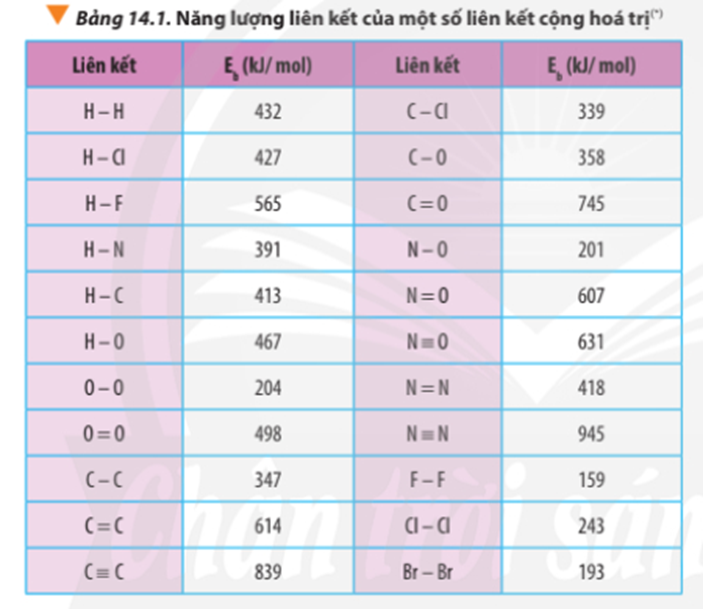
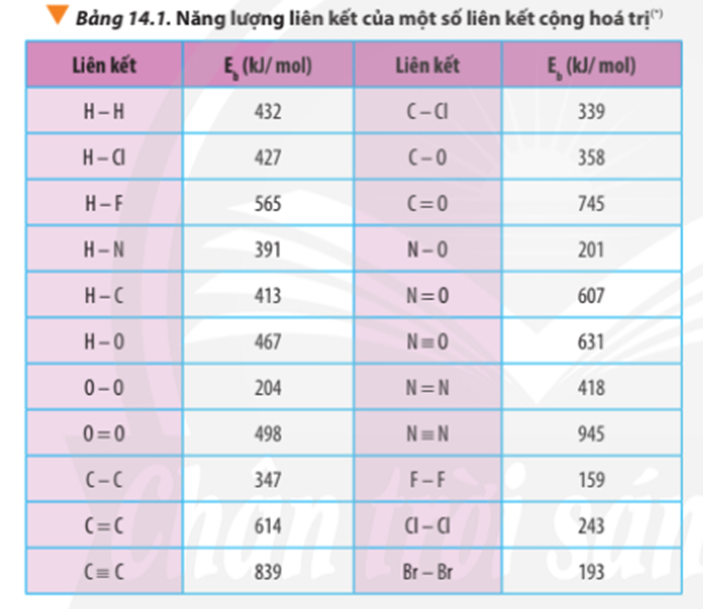
- Cách 2: Dựa vào năng lượng liên kết của các chất.
∆r = Eb(CH4) + 2.Eb(O2) – Eb(CO2) – 2.Eb(H2O)
∆r = 4.Eb(C-H) + 2.Eb(O=O) – 2. Eb(C=O) – 2.2.Eb(O-H)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(g)
Tính theo nhiệt tạo thành của hợp chất:
∆ r = 3.∆ f(CO2) + 4. ∆ f(H2O) - ∆ f(C3H8) – 5.∆ f(O2)
∆ r = 3.(-393,50) + 4.(-241,82) – (-105,00) - 5.0
∆ r = -2042,78 kJ
Tính theo năng lượng liên kết:
∆ r = Eb(C3H8) + 5.Eb(O2) – 3Eb(CO2) – 4Eb(H2O)
∆ = 2.Eb(C-C) + 8.Eb(C-H) + 5.Eb(O=O) -3.2.Eb(C=O) - 4.2.Eb(O-H)
∆ r = 2.347 + 8.413 + 5.498 – 3.2.745 – 4.2.467
∆ r = -1718 kJ
Nhận xét: Biến thiên enthalpy chuẩn của phản ứng dựa vào nhiệt tạo thành có giá trị -2 042,78 kJ âm hơn so với biến thiên enthalpy chuẩn của phản ứng dựa vào năng lượng liên kết – 1718 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.