Bài tập Định luật tuần hoàn – Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học có đáp án
47 người thi tuần này 4.6 1.3 K lượt thi 10 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi cuối kì 2 Hóa học 10 THPT Xuân Hoà (Vĩnh Phúc) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Long Hải - Phước Tỉnh (Bà Rịa - Vũng Tàu) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kẻ Sặt (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kiến Văn (Đồng Tháp) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Gia Lộc (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Điểu Cải (Đồng Nai) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Sào Nam (Quảng Nam) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Lê Lợi (Quảng Trị) năm 2023-2024 có đáp án
Danh sách câu hỏi:
Lời giải
Fluorine thuộc ô số 9, chu kì 2, nhóm VIIA trong bảng tuần hoàn (là nhóm phi kim điển hình).
Cấu hình electron của F là: 1s22s22p5 ⇒ Có 7 electron lớp ngoài cùng. Khi hình thành liên kết hóa học F có xu hướng nhận thêm 1 electron để đạt được cấu hình electron bền vững của khí hiếm ⇒ F có tính oxi hóa mạnh.
B/ Câu hỏi giữa bài
Lời giải
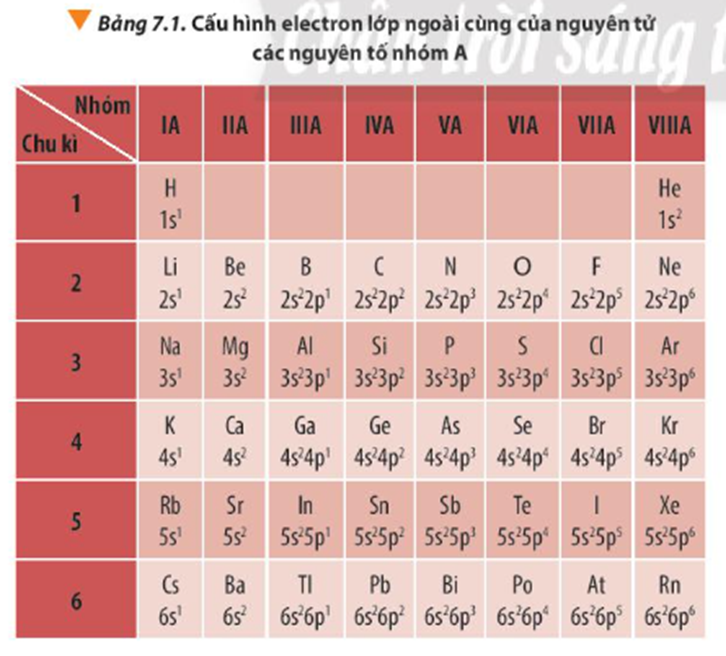
Với các nguyên tố nhóm A trong bảng tuần hoàn:
- Trong một chu kì, theo chiều tăng dần điện tích hạt nhân thì số electron lớp ngoài cùng tăng dần.
- Trong một nhóm, các nguyên tử có số electron lớp ngoài cùng bằng nhau (trừ He).
Lời giải
Xu hướng biến đổi một số tính chất của các nguyên tố, đơn chất và hợp chất:
- Bán kính nguyên tử:
+ Trong một chu kì, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử của các nguyên tố có xu hướng giảm dần.
+ Trong một nhóm, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử của các nguyên tố có xu hướng tăng.
- Độ âm điện:
+ Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, độ âm điện của nguyên tử các nguyên tố có xu hướng tăng dần.
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, độ âm điện của nguyên tử các nguyên tố có xu hướng giảm dần.
- Tính kim loại, tính phi kim:
+ Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại của các nguyên tố giảm dần, tính phi kim tăng dần.
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, tính kim loại của các nguyên tố tăng dần, tính phi kim giảm dần.
- Tính aid – base của oxide và hydroxide: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, tính acid của chúng tăng dần.
- Số electron lớp ngoài cùng trong một chu kì: Trong một chu kì, theo chiều tăng dần điện tích hạt nhân thì số electron lớp ngoài cùng tăng dần.
Lời giải
Cấu tạo nguyên tử Ca:
Cấu hình electron: 1s22s22p63s23p64s2
Số proton, số electron: 20
Số lớp electron: 4
Số electron lớp ngoài cùng: 2
Ví trí nguyên tố Ca
Số thứ tự nguyên tố: 20
Số thứ tự chu kì: 4
Nhóm: IIA
Tính chất nguyên tố Ca
Tính kim loại, tính phi kim: kim loại mạnh
Hóa trị cao nhất với oxygen: 2
Công thức oxide cao nhất: CaO
Công thức hydroxide tương ứng: Ca(OH)2
Tính acid, base của oxide cao nhất và hydroxide: base mạnh
Lời giải
a) Nguyên tố potassium thuộc ô 19.
⇒ Số hiệu nguyên tử Z = 19 = số proton = số electron.
Cấu hình electron K (Z = 19): 1s22s22p63s23p64s1.
Số lớp electron: 4.
Số electron lớp ngoài cùng: 1.
b) Nguyên tử của nguyên tố chlorine có 17 proton.
⇒ Số thứ tự nguyên tố: 17
Cấu hình electron: 1s22s22p63s23p5.
Số thứ tự chu kì = số lớp electron = 3
Số thứ tự nhóm VIIA (do 7 electron lớp ngoài cùng, nguyên tố p).
c) Nguyên tử của nguyên tố sulfur thuộc ô 16
⇒ Số hiệu nguyên tử Z = số proton = số electron = 16
Cấu hình electron: 1s22s22p63s23p4
Dựa vào cấu hình electron ta thấy nguyên tử nguyên tố sulfur có 6 electron lớp ngoài cùng
⇒ Là phi kim
Hóa trị cao nhất với oxygen là VI.
Công thức oxide cao nhất: SO3 là acidic oxide.
Công thức hydroxide tương ứng: H2SO4 là acid mạnh.
Lời giải
Potassium hydroxide (KOH) được sử dụng để sản xuất chất tẩy rửa, thuốc nhuộm vải, phân bón, … ⇒ Potassium hydroxide (KOH) hoạt động hóa học mạnh.
⇒ Dự đoán hydroxide này có tính base mạnh.
Ngoài ra, dựa vào K thuộc nhóm IA trong bảng tuần hoàn, có thể dự đoán KOH có tính base mạnh.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 4/10 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.