Bài tập Ôn tập chương 6 có đáp án
34 người thi tuần này 4.6 1.1 K lượt thi 6 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi cuối kì 2 Hóa học 10 THPT Xuân Hoà (Vĩnh Phúc) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Long Hải - Phước Tỉnh (Bà Rịa - Vũng Tàu) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kẻ Sặt (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kiến Văn (Đồng Tháp) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Gia Lộc (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Điểu Cải (Đồng Nai) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Sào Nam (Quảng Nam) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Lê Lợi (Quảng Trị) năm 2023-2024 có đáp án
Danh sách câu hỏi:
Lời giải
Tốc độ phản ứng:
Xét phản ứng hoá học dạng tổng quát: aA + bB ⟶ cC + dD.
Biểu thức tốc độ trung bình của phản ứng:
Nếu phản ứng trên là một phản ứng đơn giản thì biểu thức tốc độ phản ứng theo hằng số tốc độ phản ứng: v = k.
Các yếu tố ảnh hưởng đến tốc độ phản ứng
+ Nồng độ
+ Áp suất
+ Nhiệt độ
+ Diện tích tiếp xúc
⇒ Khi tăng các yếu tố này làm tăng số va chạm hiệu quả, dẫn đến tốc độ phản ứng tăng.
+ Chất xúc tác: Khi có chất này, năng lượng hoạt hoá giảm dẫn đến tốc độ phản ứng tăng.
Lời giải
(a) Đốt cháy nhiên liệu: xảy ra với tốc độ nhanh.
(b) Sắt bị gỉ: xảy ra với tốc độ chậm.
(c) Trung hòa acid – base: xảy ra với tốc độ nhanhLời giải
(a) Khi thay kẽm hạt bằng kẽm bột cùng khối lượng và khuấy đều thì tốc độ phản ứng tăng lên do tăng diện tích tiếp xúc của Zn.
(b) Khi thay dung dịch H2SO4 2 M bằng dung dịch H2SO4 1 M có cùng thể tích thì tốc độ phản ứng giảm do nồng độ acid giảm.
(c) Khi thực hiện phản ứng ở nhiệt độ cao hơn (khoảng 50 °C) thì tốc độ phản ứng tăng lên do số lần va chạm hiệu quả tăng.
Lời giải
a) Đồ thị mô tả sự phụ thuộc của thể tích khí oxygen theo thời gian
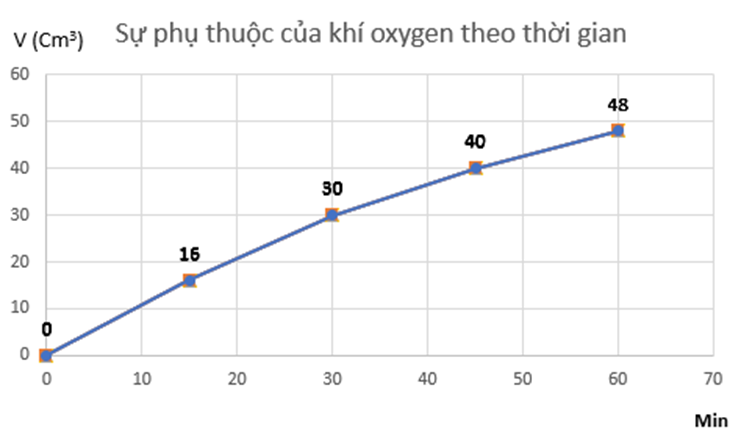
b) Tốc độ trung bình của phản ứng từ 0 ÷ 15 phút là:
cm3/min
Tốc độ trung bình của phản ứng từ 15 ÷ 30 phút là:
Tốc độ trung bình của phản ứng từ 30 ÷ 45 phút là: cm3/min
Tốc độ trung bình của phản ứng từ 45 ÷ 60 phút là: cm3/min
⇒ Tốc độ trung bình giảm dần theo thời gian.
Lời giải
Chuẩn bị: Zn dạng viên, quỳ tím, sulfuric acid loãng, 2 ống nghiệm, đèn cồn, kẹp gỗ.
Tiến hành:
- Cho vào mỗi ống nghiệm khoảng 3 mL sulfuric acid loãng.
- Cho vào mỗi ống nghiệm mẩu quỳ tím và cho vào mỗi ống 1 viên Zn.
- Đun nóng 1 ống nghiệm.
Lưu ý: Làm sạch bề mặt Zn trước khi tiến hành thí nghiệm.
Hiện tượng:
- Ban đầu, khi cho quỳ tím vào 2 ống nghiệm thì quỳ tím chuyển sang màu đỏ.
- Ống nghiệm bị đun nóng thì quỳ tím nhạt màu nhanh chóng.
Phương trình hóa học:
Zn + 2HCl ⟶ ZnCl2 + H2
Lời giải
Mở rộng:
⇒ ⇒ a = 2
⇒ T = 45 – 10.2 = 25 oC
⇒ Vậy phải giảm xuống đến 25 oC thì tốc độ phản ứng là 0,017 mol/(L.min)





















