Một mẫu chất tại thời điểm ban đầu có chứa 0,2 g đồng vị phóng xạ , có hằng số phóng xạ bằng 4,916. Biết rằng sau một khoảng thời gian nào đó, xảy ra phóng xạ và biến đổi thành hạt nhân con X.
a) Quá trình phóng xạ của là một phản ứng hạt nhân tỏa năng lượng.
b) Hạt nhân con X được tạo thành từ quá trình phóng xạ trên là .
c) Chu kì bán rã của xấp xỉ bằng 1,41. s.
d) Sau 50 triệu năm (xem như mỗi năm có 365 ngày), khối lượng còn lại trong mẫu chất đó khoảng 0,089 g.
Quảng cáo
Trả lời:
|
|
Nội dung |
Đúng |
Sai |
|
a |
Quá trình phóng xạ của là một phản ứng hạt nhân tỏa năng lượng. |
Đ |
|
|
b |
Hạt nhân con X được tạo thành từ quá trình phóng xạ trên là . |
|
S |
|
c |
Chu kì bán rã của xấp xỉ bằng 1,41. s. |
Đ |
|
|
d |
Sau 50 triệu năm (xem như mỗi năm có 365 ngày), khối lượng còn lại trong mẫu chất đó khoảng 0,089 g. |
|
S |
a) Quá trình phóng xạ luôn là phản ứng hạt nhân tỏa năng lượng.
b) Phương trình phóng xạ α của hạt nhân là:
Vậy hạt nhân X là .
c) Chu kì bán rã của là: (s).
d) Khối lượng còn lại trong mẫu chất đó sau 50 triệu năm là:
g.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
Áp dụng phương trình Clapeyron: cho khối khí cần hít vào ở điều kiện chuẩn và ở nơi đang chạy bộ lần lượt ta có:
Do khối lượng không khí hít vào trong mỗi nhịp thở được xem là bằng nhau nên .
Suy ra: Þ
Thể tích của 1 g = 1.10-3 kg không khí ở điều kiện chuẩn: m3
Thể tích không khí cần hít vào trong mỗi nhịp thở khi chạy bộ ở nơi có áp suất 200 kPa và nhiệt độ 20 0C là:
mℓ.
Lời giải
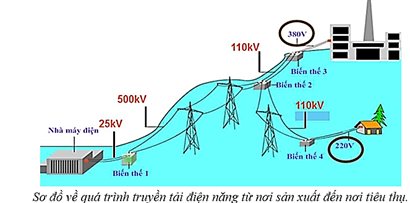
a) Trong sơ đồ về quá trình truyền tải điện năng, máy biến thế 1 là máy tăng thế. Còn máy biến thế 2, máy biến thế 3 và máy biến thế 4 là máy giảm thế.
b) Số vòng dây của cuộn dây thứ cấp ở máy biến thế 1 là:
Û vòng.
c) Công suất hao phí điện năng trên đường dây tải điện khi truyền từ nhà máy đến thành phố X là:
W.
d) Nếu không sử dụng máy biến thế 1 thì công suất hao phí điện năng trên đường dây tải điện khi truyền từ nhà máy đến thành phố X là:
W.
Lượng điện năng hao phí được giảm mỗi ngày (24 giờ):
J = 379 975,68 kW.h.
Chi phí phải chi trả cho hao phí điện năng xuất hiện trên dây tải trong mỗi ngày (24 giờ) được giảm: 379 975,68.145 » 55 096 474 đồng.
|
|
Phát biểu |
Đúng |
Sai |
|
a |
Trong sơ đồ về quá trình truyền tải điện năng, máy biến thế 1 và máy biến thế 3 là máy tăng thế. Còn máy biến thế 2 và máy biến thế 4 là máy giảm thế. |
|
S |
|
b |
Máy biến thế 1 có số vòng dây của cuộn dây thứ cấp là 20000 vòng. |
Đ |
|
|
c |
Công suất hao phí điện năng trên đường dây tải điện khi truyền từ nhà máy đến thành phố X là |
Đ |
|
|
d |
Khi có sử dụng máy biến thế 1 thì chi phí phải chi trả cho hao phí điện năng xuất hiện trên dây tải trong mỗi ngày (24 giờ) được giảm xấp xỉ 5,5 triệu đồng so với khi chưa sử dụng máy biến thế 1. Lấy giá điện 145 đồng/kW.h. |
|
S |
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
A. 225 mW.
B. 22,5 mW.
C. 90 mW.
D. 900 mW.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.