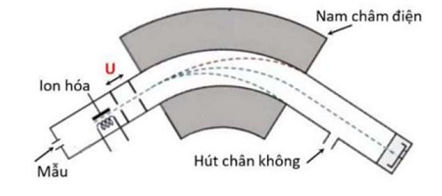
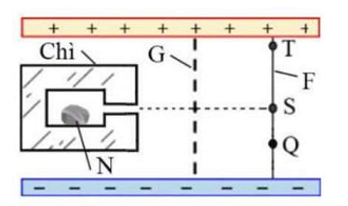
Đồng vị xenon ( \(\;_{54}^{133}{\rm{Xe}}\) ) là chất phóng xạ \({\beta ^ - }\)có chu kì bán rã là 5,24 ngày. Trong y học, hỗn hợp khí chứa xenon được sử dụng để đánh giá độ thông khí của phổi người bệnh. Một người bệnh được chỉ định sử dụng liều xenon có độ phóng xạ \(3,18 \cdot {10^8}{\rm{\;Bq}}\). Coi rằng \(85,0{\rm{\% }}\) lượng xenon trong liều đó lắng đọng tại phổi. Người bệnh được chụp ảnh phổi lần thứ nhất ngay sau khi hít khí và lần thứ hai sau đó 24,0 giờ. Biết khối lượng mol nguyên tử của xenon là \(133{\rm{\;g}}/{\rm{mol}}\).
Đồng vị xenon ( \(\;_{54}^{133}{\rm{Xe}}\) ) là chất phóng xạ \({\beta ^ - }\)có chu kì bán rã là 5,24 ngày. Trong y học, hỗn hợp khí chứa xenon được sử dụng để đánh giá độ thông khí của phổi người bệnh. Một người bệnh được chỉ định sử dụng liều xenon có độ phóng xạ \(3,18 \cdot {10^8}{\rm{\;Bq}}\). Coi rằng \(85,0{\rm{\% }}\) lượng xenon trong liều đó lắng đọng tại phổi. Người bệnh được chụp ảnh phổi lần thứ nhất ngay sau khi hít khí và lần thứ hai sau đó 24,0 giờ. Biết khối lượng mol nguyên tử của xenon là \(133{\rm{\;g}}/{\rm{mol}}\).
b) Hằng số phóng xạ của \(\;_{54}^{133}{\rm{Xe}}\) là \(0,132{\rm{\;}}{{\rm{s}}^{ - 1}}\).
Câu hỏi trong đề: Đề thi tham khảo ôn thi THPT Vật lý có đáp án - Đề 1 !!
Quảng cáo
Trả lời:
a) Đúng. \[_{54}^{133}Xe \to \,_{ - 1}^0e + \,_{55}^{133}Cs\]
b) Sai. \[\lambda = \frac{{\ln 2}}{T} = \frac{{\ln 2}}{{5,24.86400}} = 1,{53.10^{ - 6}}{s^{ - 1}}.\]
c) Đúng. \[{H_0} = \lambda {N_0} \Rightarrow 3,{18.10^8} = 1,{53.10^{ - 6}}{N_0} \Rightarrow {N_0} = 2,{08.10^{14}}\]
\[{n_0} = \frac{{{N_0}}}{{{N_A}}} = \frac{{2,{{08.10}^{14}}}}{{6,{{02.10}^{23}}}} = 3,{45.10^{ - 10}}mol\]
\[{m_0} = {n_0}M = 3,{45.10^{ - 10}}.133 = 0,0459\,\mu g\]
d) Sai. Ta có \[H = 85\% {H_0}{.2^{ - \frac{t}{T}}} = 0,85.3,{18.10^8}{.2^{ - \frac{1}{{5,24}}}} = 2,{37.10^8}Bq.\]
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Câu 1
Lời giải
Đáp án đúng là A
\[n = \frac{{pV}}{{RT}} \Rightarrow \frac{{{n_2}}}{{{n_1}}} = \frac{{{T_1}}}{T} = \frac{{25 + 273}}{{55 + 273}} \approx 0,91 = 91\% .\] Số mol khí thoát ra ngoài là 100% - 91% = 9%.
Câu 2
Công suất phát điện của một nhà máy điện hạt nhân là 1060 MW ở hiệu suất \(35{\rm{\% }}\). Coi rằng mỗi hạt nhân \(\;_{92}^{235}{\rm{U}}\) phân hạch tỏa ra năng lượng là 203 MeV . Biết \(1{\rm{eV}} = 1,60 \cdot {10^{ - 19}}{\rm{\;J}}\). Khối lượng mol nguyên tử của \(\;_{92}^{235}{\rm{U}}\) là \(235{\rm{\;g}}/{\rm{mol}}\).
Biết chỉ có \(80{\rm{\% }}\) số nguyên tử \(\;_{92}^{235}{\rm{U}}\) phân hạch. Nhà máy điện hạt nhân nói trên sẽ sử dụng hết \(220{\rm{\;kg}}\;_{92}^{235}{\rm{U}}\) trong bao nhiêu ngày (làm tròn kết quả đến chữ số hàng đơn vị)?
Lời giải
56
\(220{\rm{\;kg}}\;_{92}^{235}{\rm{U}}\) có \[N = \frac{{{{220.10}^3}}}{{235}}.6,{02.10^{23}} = 5,{64.10^{26}}\] hạt nhân.
Số nguyên tử \(\;_{92}^{235}{\rm{U}}\) phân hạch trong 1 giây là: \[80\% .5,{64.10^{26}} = 4,{51.10^{26}}\]hạt.
Theo câu 5, trong 1 giây có 9,3.1019 nguyên tử phân hạch.
Thời gian \[t = \frac{{4,{{51.10}^{26}}}}{{9,{{3.10}^{19}}}} = 4,{85.10^6}s = 56\] ngày.
Câu 3
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 4
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 5
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.