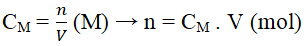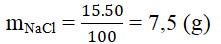Câu hỏi trong đề: Tổng hợp câu hỏi ôn tập Hóa Học lớp 8 cực hay, chi tiết !!
Quảng cáo
Trả lời:
Để pha chế một dung dịch theo nồng độ cho trước, ta thực hiện theo hai bước sau:
Bước 1. Tính các đại lượng cần dùng.
Bước 2. Pha chế dung dịch theo các đại lượng đã xác định.
a) Pha chế dung dịch theo nồng độ mol/l (CM) cho trước:
Từ muối A, nước cất và các dụng cụ cần thiết. Hãy pha chế V ml dung dịch A nồng độ CM.
+ Bước 1. Tính số mol chất tan có trong dung dịch cần pha theo công thức:
+ Bước 2. Từ số mol suy ra khối lượng chất tan A (m) cần lấy để pha chế.
+Bước 3. Tính thể tích nước cần dùng để pha chế.
Vậy cần lấy m gam chất tan A hòa tan vào V ml nước cất để tạo thành V ml dung dịch A có nồng độ CM.
Ví dụ: Từ muối NaCl, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế: 100 ml dung dịch NaCl 1M.
Hướng dẫn:
Bước 1: Tính toán:
- Số mol chất tan NaCl là:
nNaCl = 1.0,1 = 0,1 (mol)
- Khối lượng của NaCl cần lấy là:
mNaCl = nNaCl . MNaCl = 0,1.58,5 = 5,85 (g)
Bước 2: Cách pha chế dung dịch:
- Cân 5,85 g NaCl khan cho vào một cốc thủy tinh loại 200 ml.
- Cho từ từ nước cất vào cốc và khuấy nhẹ cho đủ 100 ml dung dịch.
- Ta được dung dịch NaCl 1M.
b) Pha chế dung dịch theo nồng độ phần trăm (C%) cho trước
Từ muối B, nước cất và các dụng cụ cần thiết, hãy pha chế m gam dung dịch B có nồng độ C%.
+ Bước 1. Tính khối lượng chất tan cần pha chế:
Bước 2. Tính khối lượng nước cần pha chế
mdd = mdm + mct → m2 = mdm = mdd – mct
Vậy cần lấy m1 gam chất B hòa tan vào m2 gam nước để thu được m gam dung dịch B có nồng độ C%.
Ví dụ: Từ muối NaCl, nước cất và các dụng cụ cần thiết, hãy tính toán và nêu cách pha chế: 50 g dung dịch NaCl 15%.
Hướng dẫn:
Bước 1: Tính toán:
- Khối lượng chất tan NaCl là:
- Khối lượng của dung môi (nước) là:
mdm = mdd – mct = 50 -7,5 = 42,5 (g)
Bước 2: Cách pha chế dung dịch:
- Cân 7,5 g NaCl khan cho vào một cốc thủy tinh loại 100 ml.
- Cân 42,5 g nước cất (hoặc 42,5 ml) cho vào cốc.
- Khuấy nhẹ cho NaCl tan hoàn toàn, ta được dung dịch NaCl 15%
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
- Dung dịch là hỗn hợp đồng nhất giữa dung môi và chất tan.
- Dung môi là chất có khả năng hòa tan chất khác để tạo thành dung dịch.
- Chất tan là chất bị hòa tan trong dung môi.
- Ví dụ: Đường tan trong nước tạo thành nước đường.
+ Dung dịch: nước đường
+ Dung môi: nước
+ Chất tan: đường.
Lời giải
- Độ tan là khái niệm biểu thị khối lượng chất tan trong một khối lượng dung môi.
- Độ tan (ký hiệu là S) của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
Ví dụ: ở 25oC độ tan của muối NaCl là 36 g nghĩa là trong 100 g nước có thể hòa tan tối đa 36 g muối để tạo thành dung dịch bão hòa.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.