Bài tập Liên kết cộng hóa trị có đáp án
103 người thi tuần này 4.6 2.9 K lượt thi 39 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Bài tập Thành phần của nguyên tử lớp 10 (có lời giải)
Bài tập Muối carbnate tác dụng với Hydrochloride acid lớp 10 (có lời giải)
Bài tập Basic oxide tác dụng với Hydrochloride acid lớp 10 (có lời giải)
Bài tập Kim loại tác dụng với Hydrochloride acid lớp 10 (có lời giải)
Bài tập Tính hệ số nhiệt độ Van't Hoff lớp 10 (có lời giải)
Bài tập Tính tốc độ tức thời của phản ứng lớp 10 (có lời giải)
Danh sách câu hỏi:
Lời giải
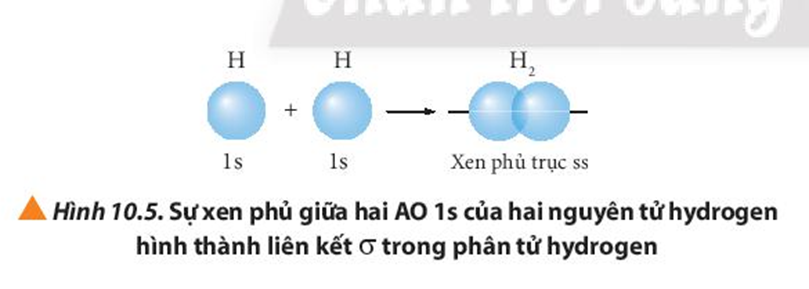
Liên kết mà các nguyên tử sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet được gọi là liên kết cộng hóa trị.
Vậy liên kết cộng hóa trị là liên kết được hình thành giữa hai nguyên tử bằng một hay nhiều cặp electron dùng chung.
Lời giải
Các nguyên tử đã góp chung electron khi tham gia hình thành liên kết để mỗi nguyên tử đều đạt được cấu hình electron bền vững giống khí hiếm với 8 electron lớp ngoài cùng.(hoặc 2 electron ở lớp ngoài cùng giống khí hiếm helium).
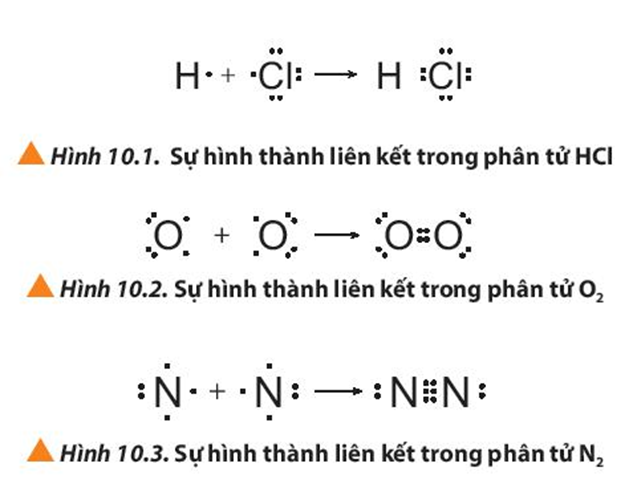
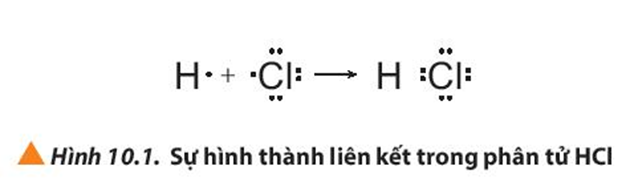
- Để tạo thành liên kết trong phân tử HCl: Nguyên tử H và Cl, mỗi nguyên tử góp chung 1 electron tạo thành 1 cặp electron dùng chung. Khi đó H đạt được cấu hình electron của khí hiếm He với 2 electron lớp ngoài cùng. Cl đạt được cấu hình electron của khí hiếm Ar với 8 electron lớp ngoài cùng.
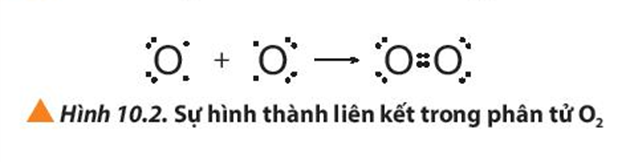
- Để tạo thành liên kết trong phân tử O2: Mỗi nguyên tử O góp chung 2 electron tạo thành 2 cặp electron dùng chung. Khi đó mỗi nguyên tử O đều đạt được cấu hình electron của khí hiếm Ne với 8 electron lớp ngoài cùng.
- Để tạo thành liên kết trong phân tử N2: Mỗi nguyên tử N góp chung 3 electron tạo thành 3 cặp electron dùng chung. Khi đó mỗi nguyên tử N đều đạt được cấu hình electron của khí hiếm Ne với 8 electron lớp ngoài cùng.
Lời giải
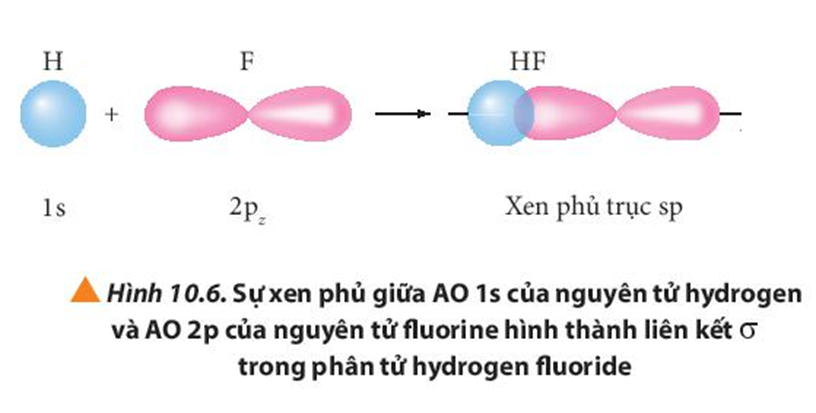
- Xét phân tử HCl:
+ Nguyên tử hydrogen (H) có cấu hình electron là 1s1, chlorine (Cl) có cấu hình electron là [Ne]3s23p5. Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử này đều cần thêm 1 electron. Vì vậy, mỗi nguyên tử H và Cl cùng góp 1 electron để tạo nên 1 cặp electron dùng chung cho cả hai nguyên tử. Lên kết giữa H và Cl được tạo nên bởi 1 cặp electron dùng chung
+ Nguyên tử oxygen (O) có cấu hình electron là 1s22s22p4 . Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử O đều cần thêm 2 electron. Vì vậy, mỗi nguyên tử O cùng góp 2 electron để tạo nên 2 cặp electron dùng chung cho cả hai nguyên tử.
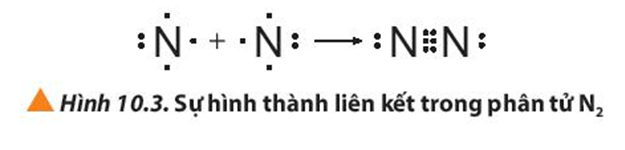
Lời giải
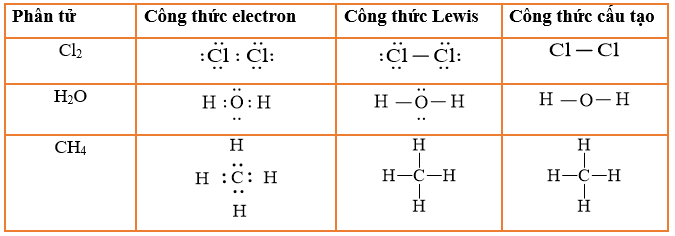
- Liên kết đơn là liên kết được tạo bởi 1 cặp electron dùng chung giữa hai nguyên tử, biểu diễn bằng một gạch nối “–”
- Liên kết đôi là liên kết được tạo bởi 2 cặp electron dùng chung giữa hai nguyên tử, biểu diễn bằng hai gạch nối “=”
- Liên kết ba là liên kết được tạo bởi 3 cặp electron dùng chung giữa hai nguyên tử, biểu diễn bằng ba gạch nối “≡”
Lời giải
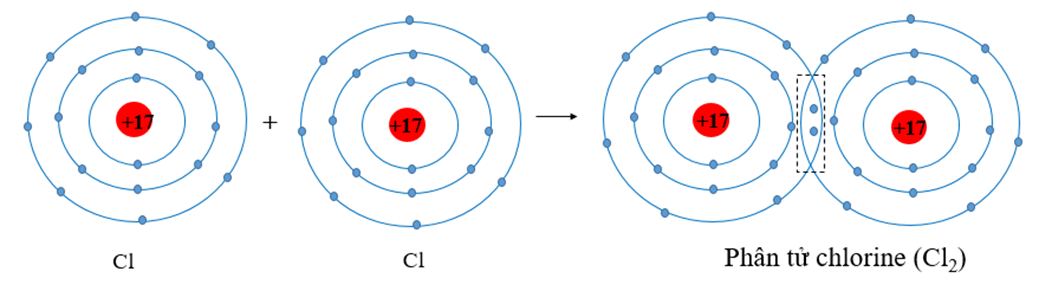
Chlorine (Cl) có cấu hình electron là [Ne]3s23p5. Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử Cl đều cần thêm 1 electron. Vì vậy, mỗi nguyên tử Cl góp chung 1 electron để tạo nên cặp electron dùng chung cho cả hai nguyên tử.
Lời giải
+ Nguyên tử nitrogen (N) có cấu hình electron là 1s22s22p3. Để đạt được cấu hình giống khí hiếm, nguyên tử N cần thêm 3 electron.
+ Nguyên tử hydrogen (H) có cấu hình electron là 1s1. Để đạt được cấu hình giống khí hiếm, nguyên tử H cần thêm 1 electron.
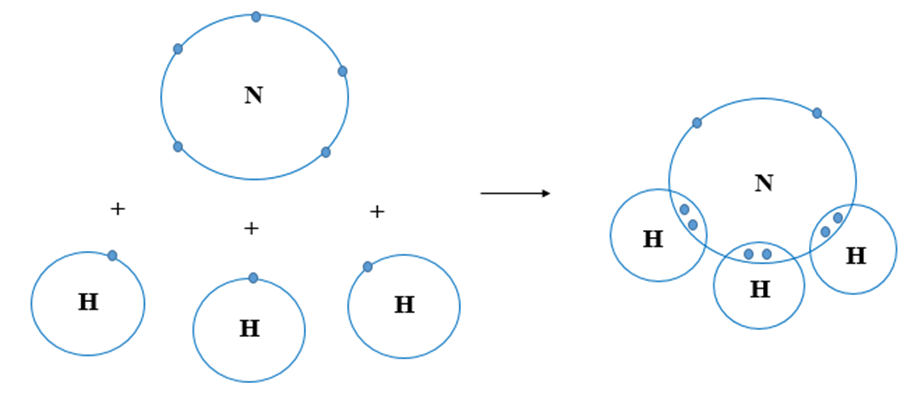
+ Để tạo thành liên kết trong phân tử NH3, mỗi nguyên tử H góp chung 1 electron với nguyên tử N tạo thành 3 cặp electron dùng chung.
Lời giải
- Cấu hình electron của O là: 1s22s22p4 ⇒ O có 6 electron ở lớp ngoài cùng ⇒ Cần nhận thêm 2 electron để đạt được cấu hình electron bền vững của khí hiếm.
- Cấu hình electron của C là: 1s22s22p2 ⇒ C có 4 elctron ở lớp ngoài cùng ⇒ Cần nhận thêm 4 electron để đạt được cấu hình electron bền vững của khí hiếm.
⇒ Mỗi nguyên tử sẽ góp chung 2 electron để tạo thành 2 cặp electron chung.
- Khi đó nguyên tử C có 6 electron (chưa đủ octet), O có 8 electron ở lớp ngoài cùng
⇒ O sẽ sử dụng 1 cặp electron chưa liên kết làm cặp electron chung với nguyên tử C. Trong CO, nguyên tử O đóng góp cặp electron chung nên nguyên là nguyên tử cho, còn nguyên tử C không đóng góp electron nên đóng vai trò nhận
⇒ Công thức electron
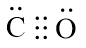
Công thức cấu tạo:
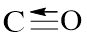
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 31/39 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.