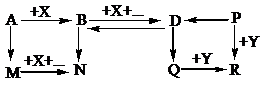
Hỗn hợp E gồm Al, Ca, Al4C3 và CaC2. Cho 15,15 gam E vào nước dư, chỉ thu được dung dịch G và hỗn hợp khí Z. Đốt cháy hết Z, thu được 4,48 lít CO2 (đktc) và 9,45 gam H2O. Nhỏ từ từ 200 ml dung dịch HCl 2M vào G, được m1 gam kết tủa. Viết các phương trình phản ứng xảy ra và tính giá trị m1.
Quảng cáo
Trả lời:
– Gọi số mol các chất trong 15,15 gam hỗn hợp E lần lượt là a, b, c, d.
– Các phản ứng xảy ra:
Ca + 2H2O →Ca(OH)2 + H2
CaC2 + 2H2O →Ca(OH)2 + C2H2
Al4C3 + 12H2O →4Al(OH)3 + 3CH4
Ca(OH)2 + 2Al + 2H2O →Ca(AlO2)2 + 3H2
Ca(OH)2 + 2Al(OH)3 →Ca(AlO2)2 + 4H2O
– Áp dụng BTNT hidro: 2nH2O(đốt cháy) = 2nH2 + 2nC2H2 + 4nCH4
2b + 12c + 2d + 3a = 0,525.2 = 1,05
2(b + d) + 3(4c + a) = 1,05 = 2nCa + 3nAl
– Xét hỗn hợp X gồm: Al, Ca, C mX = mCa + mAl + mC = 15,15 (g)
mCa + mAl = 12,75 (g) nCa = 0,15 (mol) ; nAl = 0,25 (mol)
– Sản phẩm không có kết tủa nên dung dịch gồm: Ca(AlO2)2 và Ca(OH)2
– Bảo toàn nguyên tố Ca và Al dung dịch Y có 0,125 (mol) Ca(AlO2)2 ;
0,15 – 0,125 = 0,025 (mol) Ca(OH)2 và 0,4 (mol) HCl
Ca(OH)2 + 2HCl →CaCl2 + 2H2O
Ca(AlO2)2 + 2HCl + 2H2O →2Al(OH)3 + CaCl2
3HCl + Al(OH)3 →AlCl3 + 3H2O
– Áp dụng công thức tính nhanh: nHCl = 2nCa(OH)2 + 8nCa(AlO2)2 – 3n
0,4 = 0,025.2 + 8.0,125 – 3n
m1= 78.(0,65 : 3) = 16,9 (g)
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
TRẢ LỜI:
– Công thức cấu tạo của acrylic acid là CH2=CH–COOH
– Các phương trình phản ứng:
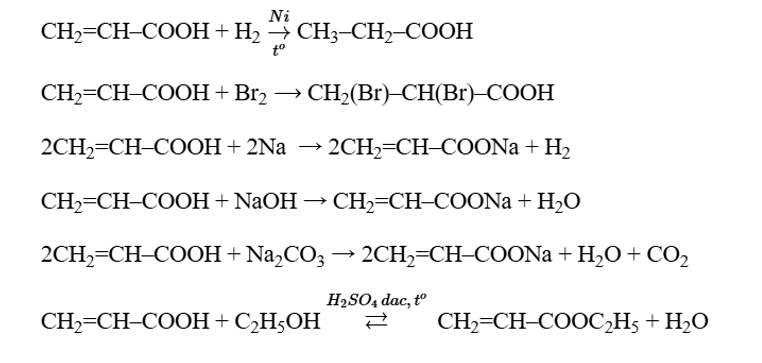
Lời giải
a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
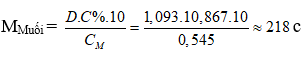
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)

2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.