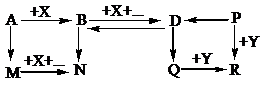
Hỗn hợp A gồm CaCO3, Cu, FeO và Al. Nung nóng A (trong điều kiện không có không khí) một thời gian thu được chất rắn B. Cho B vào nước dư, thu được dung dịch C và chất rắn D (không thay đổi khối lượng khi cho vào dung dịch NaOH). Cho D tác dụng với dung dịch H2SO4 đặc nóng, dư. Xác định thành phần của B, C, D và viết các phương trình phản ứng xảy ra.
Quảng cáo
Trả lời:
Phản ứng: CaCO3 → CaO + CO2
2Al + 3FeO →Al2O3 + 3Fe
(B gồm CaO, Cu, FeO, CaCO3 dư, Fe, Al)
CaO + H2O → Ca(OH)2
2Al + Ca(OH)2 + 2H2O →Ca(AlO2)2 + 3H2
Al2O3 + Ca(OH)2 →Ca(AlO2)2 + H2O
Do D không thay đổi khối lượng khi cho vào dung dịch NaOH, nên D không còn Al và Al2O3
Suy ra: D gồm Cu, FeO, CaCO3, Fe. Dung dịch C gồm Ca(AlO2)2, Ca(OH)2 dư.
CaCO3 + H2SO4 đặc →CaSO4 + CO2 + H2O
Cu + 2H2SO4 đặc →CuSO4 + 2H2O + SO2
2FeO + 4H2SO4 đặc →Fe2(SO4)3 + SO2 + 4H2O
2Fe + 6H2SO4 đặc → Fe2(SO4)3 + 3SO2 + 6H2O
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
TRẢ LỜI:
– Công thức cấu tạo của acrylic acid là CH2=CH–COOH
– Các phương trình phản ứng:
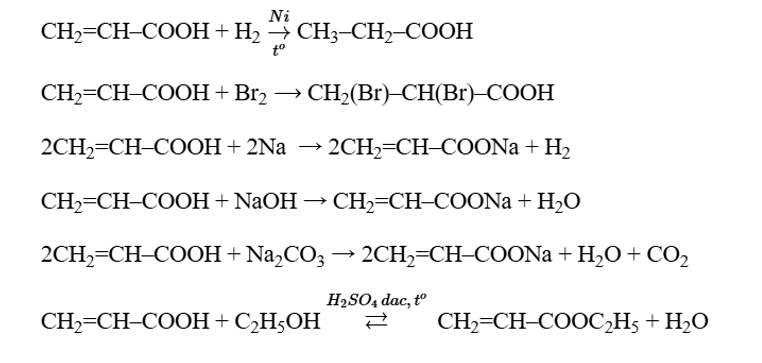
Lời giải
a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
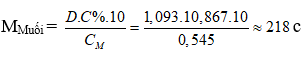
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)

2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.