(4 điểm)
Hòa tan hoàn toàn 4,8 gam magie trong 200 gam dung dịch H2SO4loãng.
a. Tính thể tích khí hiđro thoát ra ở đktc.
b. Tính nồng độ phần trăm của dung dịch H2SO4cần dùng.
c. Tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng.
d. Dẫn lượng khí hiđro ở trên qua 4,8 gam Fe2O3nung nóng. Tính khối lượng sắt tạo thành (Biết hiệu suất phản ứng 100%).
Câu hỏi trong đề: Đề thi Hóa 9 giữa kì 1 có đáp án !!
Quảng cáo
Trả lời:
a. Số mol của Mg là: nMg= = 0,2 mol
= 0,2 mol
Phương trình phản ứng:
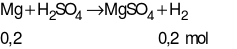
Theo phương trình phản ứng ta có: = 0,2 mol
= 0,2 mol
Suy ra thể tích khí H2thoát ra ở đktc là:
 = 0,2.22,4 = 4,48 lít
= 0,2.22,4 = 4,48 lít
b. Phương trình phản ứng:
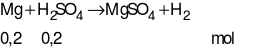
Suy ra = 0,2 mol;
= 0,2 mol; = 0,2.98 = 19,6 gam
= 0,2.98 = 19,6 gam
Vậy nồng độ phần trăm của dung dịch H2SO4cần dùng là:
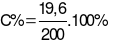 = 9,8%
= 9,8%
c. Ta có khối lượng dung dịch sau phản ứng là:
mdd sau phản ứng= 200 + 4,8 – 0,2.2 = 204,4 g
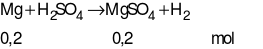
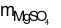 = 0,2.120 = 24 g
= 0,2.120 = 24 g
Suy ra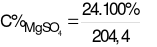 = 11,74%
= 11,74%
d. Số mol của Fe2O3là: = 0,03 mol
= 0,03 mol
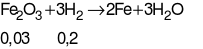
Xét tỉ lệ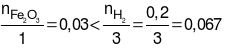
Suy ra Fe2O3hết, H2dư
Phương trình phản ứng:
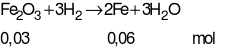
Vậy khối lượng sắt tạo thành là mFe= 0,06.56 = 3,36 gam.
Hot: 1000+ Đề thi cuối kì 2 file word cấu trúc mới 2026 Toán, Văn, Anh... lớp 1-12 (chỉ từ 60k). Tải ngay
CÂU HỎI HOT CÙNG CHỦ ĐỀ
Lời giải
CaO tiếp xúc lâu ngày với không khí sẽ bị giảm chất lượng do tác dụng với CO2, hơi nước … có trong không khí.
Phương trình hóa học:
CaO + CO2 → CaCO3
CaO + H2O → Ca(OH)2
Cho biết: Mg = 24, H = 1, S = 32, O = 16, Fe = 56
Lời giải
- Đánh số thứ tự và trích mẫu thử
- Cho quỳ tím vào 3 mẫu thử:
+ Mẫu làm quỳ tím hóa đỏ là HCl
+ Mẫu làm quỳ tím hóa xanh là NaOH
+ Mẫu không làm đổi màu quỳ là NaNO3và Na2SO4(1)
- Cho một lượng BaCl2vào nhóm (1), nếu:
+ Xuất hiện kết tủa trắng là Na2SO4
Phương trình phản ứng: BaCl2+ Na2SO4→ BaSO4(↓ trắng)+ 2NaCl
+ Không xảy ra hiện tượng gì thì đó là NaNO3.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















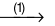 Na2O
Na2O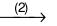 NaOH
NaOH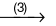 Na2CO3
Na2CO3 NaCl
NaCl NaOH.
NaOH.