12 Bài tập Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết (có lời giải)
59 người thi tuần này 4.6 1.1 K lượt thi 12 câu hỏi 45 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi cuối kì 2 Hóa học 10 THPT Xuân Hoà (Vĩnh Phúc) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Long Hải - Phước Tỉnh (Bà Rịa - Vũng Tàu) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kẻ Sặt (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kiến Văn (Đồng Tháp) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Gia Lộc (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Điểu Cải (Đồng Nai) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Sào Nam (Quảng Nam) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Lê Lợi (Quảng Trị) năm 2023-2024 có đáp án
Danh sách câu hỏi:
Câu 1/12
A. -113 kJ.
B. +113 kJ.
C. -527 kJ.
D. +527 kJ.
Lời giải
Đáp án đúng là: A
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
\[{\Delta _r}H_{298}^0 = 1 \times {E_b}(C{H_4}) + 1 \times {E_b}(C{l_2}) - 1 \times {E_b}(C{H_3}Cl) - 1 \times {E_b}(HCl)\]
= 1 × 4EC – H + 1 × ECl – Cl – 1 × (3EC – H + EC – Cl) – 1 × EH – Cl
= 1 × 4 × 414 + 1 × 243 - 1×(3×414 + 339) - 1×431 = -113 (kJ).
Câu 2/12
A. +105 kJ.
B. -105 kJ.
C. +986 kJ.
D. -986 kJ.
Lời giải
Đáp án đúng là: B
Biến thiên enthalpy chuẩn của phản ứng trên được tính theo năng lượng liên kết là
\[{\Delta _r}H_{298}^0 = 3 \times {E_b}({H_2}) + {E_b}({N_2}) - 2 \times {E_b}(N{H_3})\]
= 3 × Eb (H – H) + Eb (N ≡ N) – 2 × 3 × Eb (N – H)
= 3 × 432 + 945 - 2 × 3 × 391 = -105 kJ.
Câu 3/12
A. +158 kJ.
B. -158 kJ.
C. +185 kJ.
D. -185 kJ.
Lời giải
Đáp án đúng là: D
Biến thiên enthalpy chuẩn của phản ứng là:
\[\begin{array}{l}{\Delta _r}H_{298}^0 = {E_b}_{(H - H)} + {E_{b(Cl - Cl)}} - 2{E_{b(H - Cl)}}\\ = 436 + 243 - 2.432 = - 185(kJ).\end{array}\]
Câu 4/12
A. -560 kJ.
B. -506 kJ.
C. +560 kJ.
D. +506 kJ.
Lời giải
Đáp án đúng là: B
Biến thiên enthalpy chuẩn của phản ứng là
\({\Delta _r}H_{298}^o = {\rm{ }}2.{E_b}\left( {{H_2}} \right){\rm{ }} + {\rm{ }}{E_b}\left( {{O_2}} \right){\rm{ }}--{\rm{ }}2.{E_b}\left( {{H_2}O} \right)\)
= 2.Eb(H-H) + Eb(O=O) – 2.2.Eb(O-H) = 2.432 + 498 – 2.2.467 = -506 (kJ).
Câu 5/12
A. -3734 kJ.
B. +3734 kJ.
C. -46 kJ.
D. +46 kJ.
Lời giải
Đáp án đúng là: A
Biến thiên enthalpy chuẩn của phản ứng là
\({\Delta _r}H_{298}^o = {\rm{ }}{E_b}\left( {{C_7}{H_{16}}} \right){\rm{ }} + {\rm{ }}11.{E_b}\left( {{O_2}} \right){\rm{ }}--{\rm{ }}7.{E_b}\left( {C{O_2}} \right){\rm{ }}--{\rm{ }}8.{E_b}\left( {{H_2}O} \right)\)
= 6.Eb(C-C) + 16Eb(C-H) + 11.Eb(O=O) – 7.2.Eb(C=O) – 8.2.Eb(O-H)
= 6.347 + 16.413 + 11.498 – 7.2.745 – 8.2.467 = -3734 kJ.
Lời giải
Đáp án đúng là: C
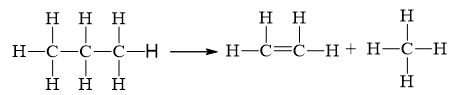
\({\Delta _r}H_{298}^o = 2.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}C} \right)}{\rm{ }} + {\rm{ }}8.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}H} \right)} - 1.{E_b}_{\left( {C{\rm{ }} = {\rm{ }}C} \right)}{\rm{ - }}8.{E_b}_{\left( {C{\rm{ }}--{\rm{ }}H} \right)}\)
= 2.346 + 8.418 - 1.612 - 8.418 = +80 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 8/12
A. -169 kJ.
B. +169 kJ.
C. -196 kJ.
D. +196 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 9/12
A. 305.
B. 360.
C. 464.
D. 837.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10/12
A. \[{\Delta _r}H_{298K}^o = m \times {\Delta _f}H_{298}^o\left( M \right) + n \times {\Delta _f}H_{298}^o\left( N \right) + a \times {\Delta _f}H_{298}^o\left( A \right) + b \times {\Delta _f}H_{298}^o\left( B \right)\]
B. \[{\Delta _r}H_{298K}^o = a \times {\Delta _f}H_{298}^o\left( A \right) + b \times {\Delta _f}H_{298}^o\left( B \right) - m \times {\Delta _f}H_{298}^o\left( M \right) - n \times {\Delta _f}H_{298}^o\left( N \right)\]
C. \[{\Delta _r}H_{298K}^o = a \times {E_b}\left( A \right) + b \times {E_b}\left( B \right) - m \times {E_b}\left( M \right) - n \times {E_b}\left( N \right)\]
D. \[{\Delta _r}H_{298K}^o = m \times {E_b}\left( M \right) + n \times {E_b}\left( N \right) - a \times {E_b}\left( A \right) - b \times {E_b}\left( B \right)\]
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11/12
A. +105 kJ.
B. -105 kJ.
C. +150 kJ.
D. -150 kJ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 12/12
A. \[{\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ + }}{\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ + }}{\Delta _f}H_{298}^0\left( {{H_2}O} \right)\]
B. \[{\Delta _f}H_{298}^0 = {\Delta _r}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ }} - {\Delta _r}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ }} - {\Delta _r}H_{298}^0\left( {{H_2}O} \right)\]
C. \[{\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right){\rm{ }} - {\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ }} - {\Delta _f}H_{298}^0\left( {{H_2}O} \right)\]
D. \[{\Delta _r}H_{298}^0 = {\rm{ }}{\Delta _f}H_{298}^0\left( {{C_2}{H_4}} \right){\rm{ + }}{\Delta _f}H_{298}^0\left( {{H_2}O} \right) - {\Delta _f}H_{298}^0\left( {{C_2}{H_5}OH} \right)\]
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 6/12 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















