Bài tập Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học có đáp án
29 người thi tuần này 4.6 2 K lượt thi 17 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi cuối kì 2 Hóa học 10 THPT Xuân Hoà (Vĩnh Phúc) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Long Hải - Phước Tỉnh (Bà Rịa - Vũng Tàu) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kẻ Sặt (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Kiến Văn (Đồng Tháp) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Gia Lộc (Hải Dương) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Điểu Cải (Đồng Nai) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Sào Nam (Quảng Nam) năm 2023-2024 có đáp án
Đề thi cuối kì 2 Hóa học 10 THPT Lê Lợi (Quảng Trị) năm 2023-2024 có đáp án
Danh sách câu hỏi:
Lời giải
Giả sử đốt cháy hoàn toàn 1 gam C và 1 gam Al ta có:
Đốt cháy hoàn toàn 1 mol C tỏa ra 393,5 kJ nhiệt lượng
Nếu đốt cháy hoàn toàn mol C tỏa ra 393,5. = 32,79 kJ nhiệt lượng
Đốt cháy hoàn toàn 2 mol Al tỏa ra 1675,7 kJ nhiệt lượng
Nếu đốt cháy hoàn toàn mol Al tỏa ra . = 31,03 kJ nhiệt lượng
Vật với cùng một khối lượng C và Al, khi đốt cháy C tỏa ra nhiều nhiệt hơn.
Lời giải
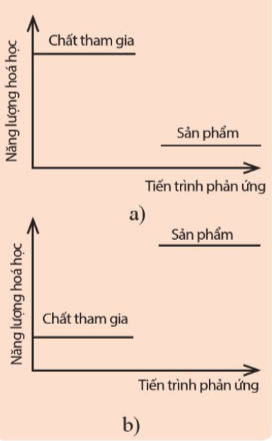
Hình a) năng lượng của hệ chất tham gia cao hơn năng lượng của hệ sản phẩm ⇒ Phản ứng diễn ra kèm theo sự giải phóng năng lượng dưới dạng nhiệt ⇒ Phản ứng tỏa nhiệt.
Hình b) năng lượng của hệ chất tham gia thấp hơn năng lượng của hệ sản phẩm ⇒ Phản ứng diễn ra kèm theo sự hấp thu năng lượng dưới dạng nhiệt ⇒ Phản ứng thu nhiệt.
Lời giải
Để đốt cháy 1 mol CH4(g) cần hấp thu 249,9 kJ nhiệt lượng
Vậy đốt cháy mol CH4(g) cần hấp thu 249,9. = 41,65 kJ nhiệt lượng.
Lời giải
Nước mắm là hỗn hợp của muối với các axit amin được chuyển biến từ protein trong thịt cá qua một quá trình thủy phân với tác nhân là các hệ enzim có sẵn trong ruột cá cùng với một loại vi khuẩn kị khí chịu mặn, nhờ các men chất đạm từ cá được cắt nhỏ thành các axit amin giúp cơ thể hấp thu trực tiếp và dễ dàng. Trong nước mắm cốt có chứa rất nhiều đạm giúp cung cấp năng lượng, giữ ấm cơ thể.
Thực tế chứng minh trước khi lặn xuống nước uống nước mắm cốt giúp cơ thể người lặn nóng lên, xuống nước không còn thấy giá rét, tránh được nguy cơ cảm lạnh. Nước mắm cốt giúp tăng sức, giữ ấm cơ thể khi lặn xuống mực nước sâu.
Lời giải
Khi đốt cháy tờ giấy hay đốt lò than, ta cần thực hiện giai đoạn khơi mào bằng cách nhóm lửa (đốt một góc tờ giấy trước, đốt cháy một góc lò than trước).
Lời giải
Khi nung vôi người ta phải xếp đá vôi lẫn với than trong lò vì:
- Phản ứng đốt cháy than là phản ứng tỏa nhiệt.
- Phản ứng nung vôi là phản ứng thu nhiệt.
- Nhiệt tỏa ra trong quá trình đốt cháy than sẽ cung cấp cho quá trình nung vôi.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 11/17 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.