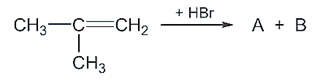Chuyên đề Hóa 12 KNTT Bài 3: Cơ chế phản ứng cộng có đáp án
31 người thi tuần này 4.6 1.2 K lượt thi 5 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Trắc nghiệm Ôn tập chương 8 lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Một số tính chất và ứng dụng của phức chất lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Sơ lược về phức chất lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Đại cương về kim loại chuyển tiếp dãy thứ nhất lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Ôn tập chương 7 lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Nguyên tố nhóm IIA lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Nguyên tố nhóm IA lớp 12 (có đúng sai, trả lời ngắn)
Trắc nghiệm Ôn tập chương 6 lớp 12 (có đúng sai, trả lời ngắn)
Danh sách câu hỏi:
Lời giải
* Phản ứng cộng được kí hiệu bằng chữ A (chữ cái đầu của từ tiếng Anh là Addition, nghĩa là cộng).
- Phản ứng cộng với tác nhân electrophile được kí hiệu là AE. Phản ứng cộng electrophile AE vào nối đôi >C = C< xảy ra qua hai giai đoạn chính:
+ Ở giai đoạn 1, liên kết đôi phản ứng với tác nhân electrophile, hình thành carbocation.
+ Ở giai đoạn 2, carbocation kết hợp với anion hình thành sản phẩm.
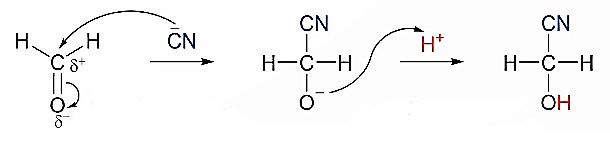
- Phản ứng cộng với tác nhân nucleophile được kí hiệu là AN.
+ Ở giai đoạn 1, liên kết đôi phản ứng với tác nhân nucleophile, hình thành cacbanion.
+ Ở giai đoạn 2, cacbanion kết hợp với cation hình thành sản phẩm.
*Sự hình thành sản phẩm chính của phản ứng cộng hydrogen halide (HCl, HBr), H2O vào alkene được giải thích theo quy tắc cộng Markovnikov: Phản ứng cộng HX (như HBr, HCl, HI, HOH, …) vào alkene không đối xứng, nguyên tử hydrogen sẽ ưu tiên cộng vào nguyên tử carbon có nhiều hydrogen hơn và X sẽ cộng vào nguyên tử carbon có ít hydrogen hơn.
Lời giải
a) Vận dụng quy tắc cộng Markovnikov xác định được sản phẩm chính: nguyên tử hydrogen sẽ ưu tiên cộng vào nguyên tử carbon có nhiều hydrogen hơn và X sẽ cộng vào nguyên tử carbon có ít hydrogen hơn.
Vậy chất A là: \(\begin{array}{l}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,Br\\C{H_3} - \mathop C\limits_{\left| {} \right.}^{\left| {} \right.} - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\); chất B là \[\begin{array}{l}C{H_3} - \mathop C\limits_{\left| {} \right.} H - C{H_2} - Br\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\].
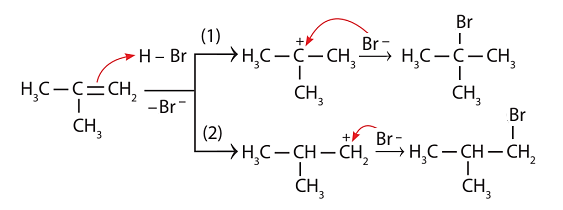
b) Cơ chế phản ứng:
Lời giải
a) Phương trình hoá học:
\(\begin{array}{l}\,C{H_2} = \mathop C\limits_{\left| {} \right.} - C{H_3} + \,{H_2}O \to \\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\)\(\left\langle \begin{array}{l}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,OH\\C{H_3} - \mathop C\limits_{\left| {} \right.}^{\left| {} \right.} - C{H_3}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(spc)\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\\C{H_3} - \mathop C\limits_{\left| {} \right.}^{} H - C{H_2} - OH\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array} \right.\)
Cơ chế phản ứng:
![Viết phương trình hoá học của phản ứng và cơ chế tạo thành sản phẩm chính khi cho các hợp chất dưới đây tác dụng với nước (có mặt H2SO4 loãng). \(\begin{array}{l}a)\,C{H_2} = \mathop C\limits_{\left| {} \right.} - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\) \[\begin{array}{l}b)\,C{H_3} - C{H_2} - \mathop C\limits_{\left| {} \right.} = CH - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\] (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2024/07/blobid2-1721479658.png)
b) Phương trình hoá học:
\[\begin{array}{l}\,C{H_3} - C{H_2} - \mathop C\limits_{\left| {} \right.} = CH - C{H_3} + {H_2}O\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\]\[ \to \left\langle \begin{array}{l}C{H_3} - C{H_2} - \mathop C\limits_{\left| {} \right.} H - \mathop C\limits_{\left| {} \right.} H - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\,\,\,\,\,OH\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,OH\\C{H_3} - C{H_2} - \mathop {\mathop C\limits^{\left| {} \right.} }\limits_{\left| {} \right.} - C{H_2} - C{H_3}\,(spc)\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array} \right.\]
Cơ chế phản ứng:
![Viết phương trình hoá học của phản ứng và cơ chế tạo thành sản phẩm chính khi cho các hợp chất dưới đây tác dụng với nước (có mặt H2SO4 loãng). \(\begin{array}{l}a)\,C{H_2} = \mathop C\limits_{\left| {} \right.} - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\) \[\begin{array}{l}b)\,C{H_3} - C{H_2} - \mathop C\limits_{\left| {} \right.} = CH - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\] (ảnh 2)](https://video.vietjack.com/upload2/quiz_source1/2024/07/blobid3-1721479664.png)
Lời giải
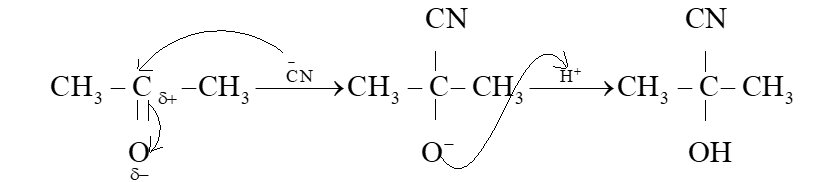
Phản ứng giữa acetone và HCN:
Cơ chế phản ứng:
Lời giải
Để viết được cơ chế phản ứng cộng electrophile vào phân tử alkene và cơ chế phản ứng cộng nucleophile vào nhóm carbonyl học sinh cần nắm được các kiến thức sau:
- Phản ứng cộng electrophile AE vào nối đôi >C = C< xảy ra qua hai giai đoạn chính:
+ Ở giai đoạn 1, liên kết đôi phản ứng với tác nhân electrophile, hình thành carbocation.
+ Ở giai đoạn 2, carbocation kết hợp với anion hình thành sản phẩm.
Ví dụ:
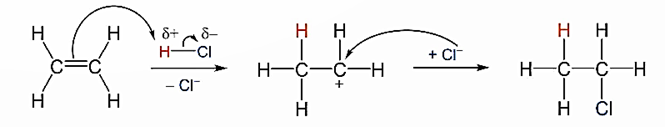
Sự hình thành sản phẩm chính của phản ứng cộng hydrogen halide (HCl, HBr), H2O vào alkene được giải thích theo quy tắc cộng Markovnikov: Phản ứng cộng HX (như HBr, HCl, HI, HOH, …) vào alkene không đối xứng, nguyên tử hydrogen sẽ ưu tiên cộng vào nguyên tử carbon có nhiều hydrogen hơn và X sẽ cộng vào nguyên tử carbon có ít hydrogen hơn.
- Phản ứng cộng hydrogen cyanide (HCN) vào hợp chất carbonyl là phản ứng cộng nucleophile (AN). Ví dụ: