Bộ 10 Đề kiểm tra Hóa 11 học kì 1 có đáp án (đề 8)
35 người thi tuần này 4.6 4.5 K lượt thi 22 câu hỏi 45 phút
🔥 Đề thi HOT:
15 câu Trắc nghiệm Hóa học 11 Kết nối tri thức Bài 15: Alkane có đáp án
15 câu Trắc nghiệm Hóa 11 Kết nối tri thức Bài 20: Alcohol có đáp án
37 câu Trắc nghiệm Hóa 11 Cánh diều Chủ đề 5: Dẫn xuất Halogen - Alcohol - Phenol
15 câu Trắc nghiệm Hóa 11 Kết nối tri thức Bài 19: Dẫn xuất halogen có đáp án
15 câu Trắc nghiệm Hóa học 11 Kết nối tri thức Bài 16: Hydrocarbon không no có đáp án
15 câu Trắc nghiệm Hóa 11 Kết nối tri thức Bài 21: Phenol có đáp án
30 câu Trắc nghiệm Hóa 11 Cánh diều Bài 18: Hợp chất carbonyl có đáp án
30 câu Trắc nghiệm Hóa 11 Cánh diều Bài 16. Alcohol có đáp án
Nội dung liên quan:
Danh sách câu hỏi:
Lời giải
Đáp án C
Khí CO2 được tạo ra từ bình chữa cháy và dùng để sản xuất đá khô.
Câu 2
Cho m gam Al phản ứng hoàn toàn với dung dịch HNO3 loãng (dư), thu được 4,48 lít khí NO (đktc, sản phẩm khử duy nhất). Giá trị của m là
Lời giải
Đáp án D
Phương trình hóa học:
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Ta có:
Áp dụng định luật bảo toàn electron:
⟹ m = 0,2.27 = 5,4 gam
Lời giải
Đáp án A
Khí amoniac làm giấy quỳ tím ẩm chuyển thành màu xanh vì:
NH3 + H2O
⟹ Môi trường bazơ.
Lời giải
Đáp án D
Phản ứng xảy giữa cặp chất NaHCO3 và NaOH có phương trình ion là:
Lời giải
Đáp án D
Các nguyên tử thuộc nhóm IVA có cấu hình electron lớp ngoài cùng là ns2np2.
Lời giải
Đáp án B
Al, Fe bị thụ động trong HNO3 đặc, nguội.
Lời giải
Đáp án B
3NH3 + 3H2O + AlCl3 → Al(OH)3↓ + 3NH4Cl
Lời giải
Đáp án A
Lời giải
Đáp án B
Tất cả các muối amoni đều dễ tan trong nước, khi tan điện li hòa toàn thành cation amoni và anion gốc axit.
Lời giải
Đáp án B
Phương trình hóa học:
3Mg + 2P Mg3P2
Lời giải
Đáp án D
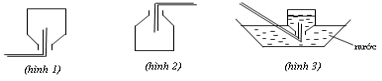
Hình 1 được áp dụng để thu khí nhẹ hơn không khí.
Hình 2 được áp dụng để thu khí nặng hơn không khí.
Hình 3 được áp dụng để thu khí không tan hoặc ít tan trong nước.Lời giải
Đáp án A
Khi nhiệt phân các muối AgNO3 hay Hg(NO3)2 đều sinh ra kim loại, khí NO2 và khí O2.
Lời giải
Đáp án A
Độ dinh dưỡng của phân lân được tính bằng % về khối lượng của P2O5 trong phân.Lời giải
Đáp án C
Chất điện li yếu là CH3COOH.
Phương trình điện li: CH3COOH ⇄
Câu 15
Cho dung dịch KOH đến dư vào 50 ml (NH4)2SO4 1M. Đun nóng nhẹ, thu được thể tích khí thoát ra (đktc) là
Cho dung dịch KOH đến dư vào 50 ml (NH4)2SO4 1M. Đun nóng nhẹ, thu được thể tích khí thoát ra (đktc) là
Lời giải
Đáp án D
Phương trình hóa học:
2KOH + (NH4)2SO4 →2NH3 + K2SO4 + 2H2O
⟹
⟹ lít
Lời giải
Đáp án D
Ta có:
Nhận thấy: ⟹ Sau phản ứng thu được chứa Ba(OH)2 dư và chất rắn BaCO3.
Lời giải
Đáp án B
Liên kết xích-ma là liên kết đơn. Liên kết đơn gồm C – C và C – H.
Số liên kết C – C là 4 – 1 = 3 liên kết.
Số liên kết C – H là 10 liên kết.
⟹ Tổng có 13 liên kết xích – ma.
Lời giải
Đáp án A
Các chất là đồng phân của nhau khi có cùng công thức phân tử và khác nhau về công thức cấu tạo.
Các chất ở đáp án có cùng công thức phân tử là C3H8O.
Lời giải
Đáp án D
Dẫn xuất hidrocacbon là hợp chất hữu cơ ngoài chứa nguyên tố C và H còn chứa các nguyên tố khác như O, N, S, halogen, ...
Lời giải
Đáp án B
Câu 21
Cho 2,8 gam N2 tác dụng H2 lấy dư. Biết hiệu suất phản ứng đạt 20%. Tính thể tích của NH3 thu được sau phản ứng (đktc)?
Cho 2,8 gam N2 tác dụng H2 lấy dư. Biết hiệu suất phản ứng đạt 20%. Tính thể tích của NH3 thu được sau phản ứng (đktc)?
Lời giải
Phương trình hóa học:
N2 + 3H2 2NH3
⟹ Theo phương trình:
Do hiệu suất phản ứng đạt 20% nên lượng NH3 sinh ra thực tế là:
Thể tích khí NH3 thu được là: V = 0,04.22,4 = 0,896 lít
Câu 22
Chia 19,4 gam hỗn hợp gồm Mg, Al, Zn thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một trong O2 dư thu được 15,7 gam hỗn hợp oxit. Phần hai hòa tan trong dung dịch HNO3 đặc, nóng dư thu được V (lít) NO2 (sản phẩm khử duy nhất, (đktc)). Tính giá trị của V.
Chia 19,4 gam hỗn hợp gồm Mg, Al, Zn thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một trong O2 dư thu được 15,7 gam hỗn hợp oxit. Phần hai hòa tan trong dung dịch HNO3 đặc, nóng dư thu được V (lít) NO2 (sản phẩm khử duy nhất, (đktc)). Tính giá trị của V.
Lời giải
Ta có: m1 = m2 = gam
- Phần 1: Phản ứng với oxi
Số mol oxi phản ứng là:
Các quá trình nhường, nhận electron
Al → + 3e
Mg → + 2e
Zn → + 2e.
Bảo toàn electron ta có:
ne nhường = ne nhận ⟹ ne nhường = 0,1875.4 = 0,75 (1)
- Phần 2: hoàn tan trong dung dịch HNO3
Các quá trình nhường, nhận electron
Al → + 3e
Mg → + 2e
Zn → + 2e.
Gọi số mol khí NO2 là a mol.
Ta có: ne nhường = ne nhận ⟹ ne nhường = a (2)
Từ (1) và (2) ⟹ 0,75 = a
⟹ lít
900 Đánh giá
50%
40%
0%
0%
0%