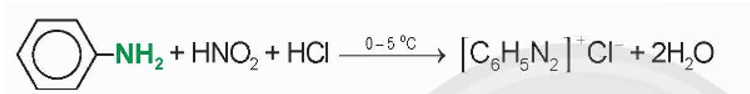Giải SGK Hóa học 12 CTST Bài 6: Amine có đáp án
33 người thi tuần này 4.6 1 K lượt thi 23 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 2
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 1
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 2
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 1
Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 2
Danh sách câu hỏi:
Lời giải
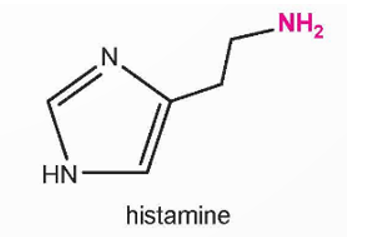
- Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon.
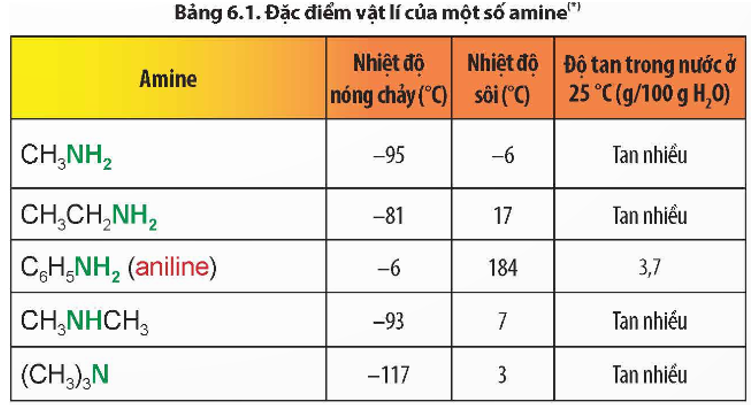
- Tính chất vật lí của amine: Ở điều kiện thường, amine có thể tồn tại ở thể khí, lỏng hoặc rắn. Nhiệt độ nóng chảy, nhiệt độ sôi của các amine cùng bậc có xu hướng tăng khi phân tử khối tăng. Các amine có số nguyên tử carbon nhỏ thường tan nhiều trong nước.
- Tính chất hoá học của amine: Amine có tính base và phản ứng tạo phức; phản ứng với nitrous acid; ngoài ra, aniline phản ứng được với nước bromine.
- Ứng dụng của amine: Amine được ứng dụng trong nhiều lĩnh vực công nghiệp, nông nghiệp, dược phẩm, thuốc nhuộm và sản xuất vật liệu.
Lời giải
Nhóm chức đặc trưng trong phân tử amine là nhóm chức amine (−NH2 hoặc −NH− hoặc > N −)
Lời giải
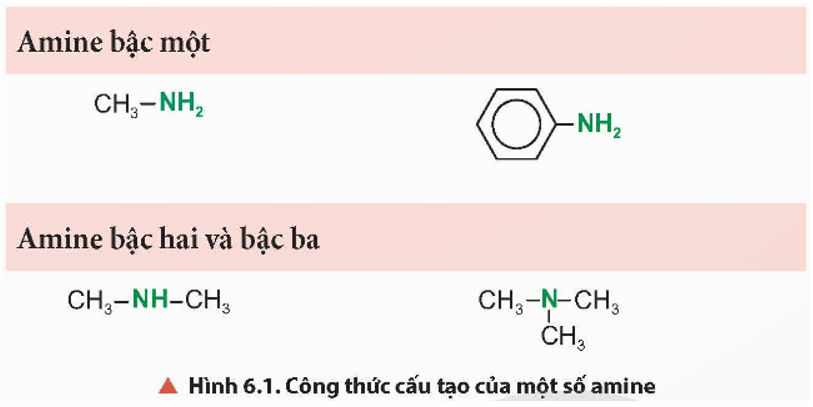
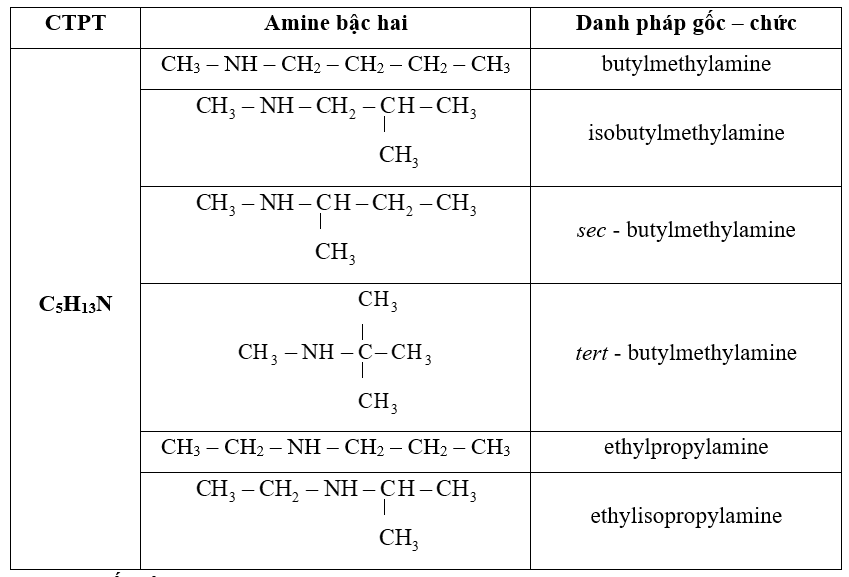
- Dựa vào số nguyên tử hydrogen của phân tử NH3 bị thay thế amine được phân loại thành: amine bậc một, amine bậc hai và amine bậc ba.
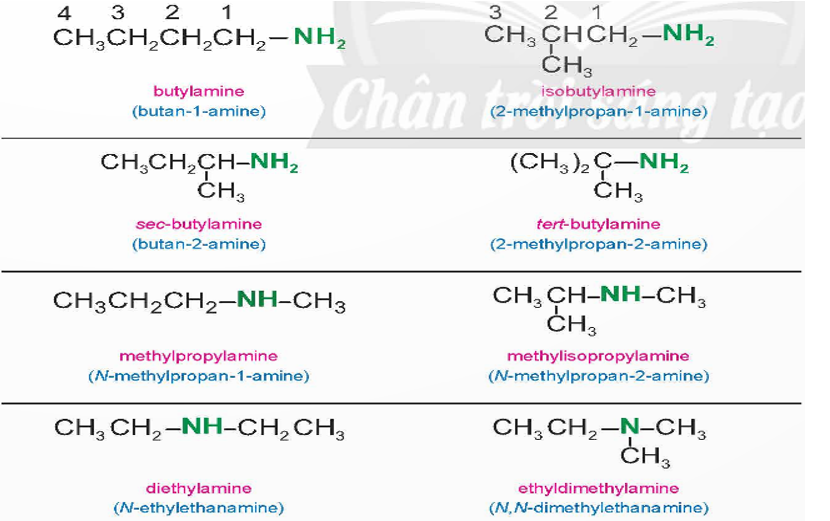
- Dựa vào đặc điểm cấu tạo của nhóm thế amine được phân thành nhiều loại trong đó điển hình là: alkylamine (nhóm amine liên kết với gốc alkyl) và arylamine (nhóm amine liên kết trực tiếp với nguyên tử carbon của vòng benzene).
- Bậc của amine được tính bằng số gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
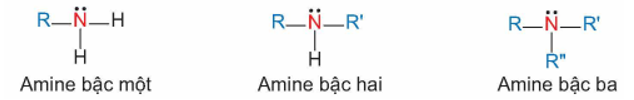
+ Amine bậc một: có 1 gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
+ Amine bậc hai: có 2 gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
+ Amine bậc ba: có 3 gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
Lời giải
- Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon. Vậy chất thuộc loại amine là: CH3 – CH2 – NH2.
- Đây là amine bậc I do có 1 gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
Lời giải
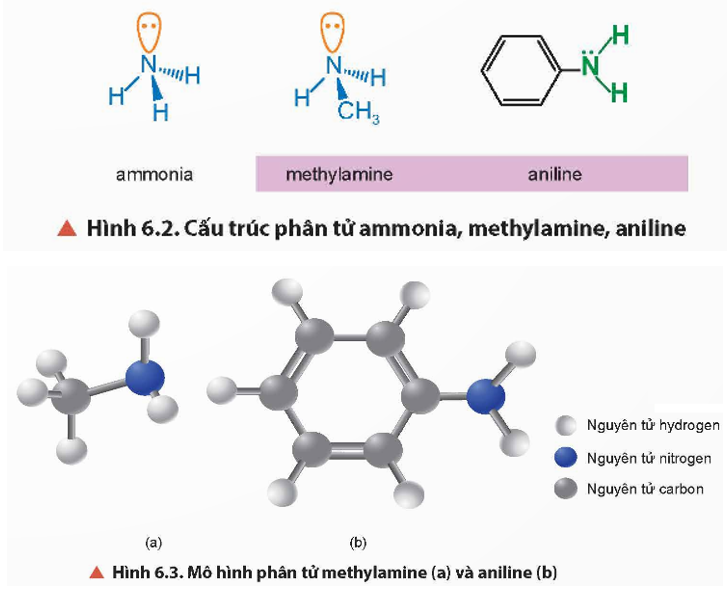
Tương tự như ammonia, nguyên tử nitrogen trong phân tử methylamine và aniline tạo 3 liên kết cộng hoá trị với hydrogen hoặc gốc hydrocarbon và có một cặp electron chưa liên kết.
Lời giải
- Ở điều kiện thường methylamine, ethylamine, dimethylamine, trimethylamine tồn tại ở thể khí.
- Nhiệt độ nóng chảy, nhiệt độ sôi của các amine có xu hướng tăng khi phân tử khối tăng.
- Khả năng hoà tan trong nước của các amine có xu hướng giảm khi phân tử khối tăng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 18/23
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 19/23
Khói thuốc lá và thuốc lá điện tử chứa các thành phần nicotine, carbon monoxide, benzene, formaldehyde, acetaldehyde, hydrogen cyanide, ... là những chất tác động trực tiếp lên não, thần kinh, tim mạch, hệ hô hấp và nguy cơ dẫn đến ung thư. Một số bạn trẻ cho rằng hút thuốc là “sành điệu”, thuốc lá điện tử không gây hại, . . . Hãy nêu quan điểm của em.

Khói thuốc lá và thuốc lá điện tử chứa các thành phần nicotine, carbon monoxide, benzene, formaldehyde, acetaldehyde, hydrogen cyanide, ... là những chất tác động trực tiếp lên não, thần kinh, tim mạch, hệ hô hấp và nguy cơ dẫn đến ung thư. Một số bạn trẻ cho rằng hút thuốc là “sành điệu”, thuốc lá điện tử không gây hại, . . . Hãy nêu quan điểm của em.

Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 15/23 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.