Chuyên đề Hóa 12 CTST Bài 2: Một số cơ chế phản ứng trong hóa học hữu cơ có đáp án
45 người thi tuần này 4.6 1.6 K lượt thi 15 câu hỏi
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 2
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 1
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 2
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 1
Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 2
Danh sách câu hỏi:
Lời giải
Để viết được cơ chế phản ứng của một số phản ứng hoá học hữu cơ phổ biến phải:
- Nắm vững được các khái niệm: tác nhân electrophile, tác nhân nucleophile …
- Trình bày được một số cơ chế phản ứng trong hoá học hữu cơ như: cơ chế thế gốc SR (vào carbon no của alkane), cơ chế cộng electrophile AE (vào liên kết đôi C=C của alkene), cơ chế thế electrophile SEAr (vào nhân thơm), cơ chế thế nucleophile SN1, SN2 (phản ứng thuỷ phân dẫn xuất halogen), cơ chế cộng nucleophile AN (vào hợp chất carbonyl)…
- Hiểu được sự tạo thành sản phẩm và hướng của một số phản ứng (cơ chế thế gốc SR vào carbon no của alkane và cơ chế cộng electrophile AE vào liên kết đôi C = C của alkene theo quy tắc cộng Markovnikov).
Lời giải
- Tác nhân electrophile là tác nhân có ái lực với electron, chúng thường là các tiểu phân mang điện tích dương (như \({H^ + },B{r^ + },{}^ + N{O_2},...\)) hoặc có trung tâm mang một phần điện tích dương (như \(\mathop C\limits^{\delta + } {H_3} - \mathop {Br}\limits^{\delta - } ,...\))
- Tác nhân nucleophile là tác nhân có ái lực với hạt nhân, chúng thường là các tiểu phân mang điện tích âm (như \(C{l^ - },H{O^ - },C{N^ - },...\)) hoặc có cặp electron hoá trị tự do (như H2O, CH3OH, …)
Như vậy:
- Trong phản ứng (1) H+ là tác nhân electrophile;
- Trong phản ứng (2) −OH là tác nhân nucleophile.
Lời giải
Xét phản ứng hữu cơ tổng quát:
Chất phản ứng + Tác nhân phản ứng → Sản phẩm
Trong phản ứng hoá học hữu cơ, chất phức tạp hơn thường được gọi là chất phản ứng; chất hữu cơ đơn giản hơn hoặc chất vô cơ thường được gọi là tác nhân phản ứng.
Lời giải
Xét phản ứng của methane với chlorine:
Phản ứng trên xảy ra theo cơ chế thế gốc tự do (SR) gồm 3 giai đoạn:
Giai đoạn khơi mào:
Giai đoạn phát triển mạch:
\(C{l^ \bullet } + C{H_4} \to \mathop C\limits^ \bullet {H_3} + HCl\)
\(\mathop C\limits^ \bullet {H_3} + C{l_2} \to C{H_3}Cl + C{l^ \bullet }\)
…
Giai đoạn tắt mạch:
\[\mathop C\limits^ \bullet {H_3} + \mathop C\limits^ \bullet {H_3} \to C{H_3} - C{H_3}\]
\(C{l^ \bullet } + C{l^ \bullet } \to C{l_2}\)
Vậy các gốc tự do tạo thành trong phản ứng của methane với chlorine là: \(C{l^ \bullet };\,\mathop C\limits^ \bullet {H_3}.\)
Lời giải
* Cơ chế phản ứng: Phản ứng trên xảy ra theo cơ chế thế gốc (SR), gồm ba giai đoạn chính như sau:
- Giai đoạn khơi mào phản ứng:
- Giai đoạn phát triển mạch phản ứng:
\(C{H_3} - C{H_2} - C{H_2} - H + B{r^ \bullet } \to C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2} + HBr\)
\(C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2} + Br - Br \to C{H_3} - C{H_2} - C{H_2} - Br + B{r^ \bullet }\)
\[\begin{array}{l}C{H_3} - \mathop C\limits_{\left| {} \right.} H - C{H_3} + B{r^ \bullet } \to C{H_3} - \mathop C\limits^ \bullet H - C{H_3} + HBr\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,H\end{array}\]
\(\begin{array}{l}C{H_3} - \mathop C\limits^ \bullet H - C{H_3} + Br - Br \to C{H_3} - \mathop C\limits_{\left| {} \right.} H - C{H_3} + B{r^ \bullet }\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,Br\end{array}\)
…..
- Giai đoạn tắt mạch phản ứng:
\(B{r^ \bullet } + {}^ \bullet Br \to Br - Br\)
\(C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2} + B{r^ \bullet } \to C{H_3} - C{H_2} - C{H_2} - Br\)
\(\begin{array}{l}C{H_3} - \mathop C\limits^ \bullet H - C{H_3} + B{r^ \bullet } \to C{H_3} - \mathop C\limits_{\left| {} \right.} H - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,Br\end{array}\)
\(C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2} + \mathop C\limits^ \bullet {H_2} - C{H_2} - C{H_3} \to C{H_3} - C{H_2} - C{H_2} - C{H_2} - C{H_2} - C{H_3}\)
\[\begin{array}{l}C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2} + C{H_3} - \mathop C\limits^ \bullet H - C{H_3} \to C{H_3} - C{H_2} - C{H_2} - \mathop C\limits_{\left| {} \right.} H - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\end{array}\]
\(\begin{array}{l}C{H_3} - \mathop C\limits^ \bullet H - C{H_3} + C{H_3} - \mathop C\limits^ \bullet H - C{H_3} \to C{H_3} - \mathop C\limits_{\left| {} \right.} H - \mathop C\limits_{\left| {} \right.} H - C{H_3}\\\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,C{H_3}\,\,\,\,\,C{H_3}\end{array}\)
* Như vậy, các gốc tự do được tạo thành: \[C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2};\,C{H_3} - \mathop C\limits^ \bullet H - C{H_3}\]
Độ bền của gốc tự do phụ thuộc vào bậc của nguyên tử carbon chứa electron độc thân.
Ta có độ bền của các gốc tự do này như sau:
\[C{H_3} - C{H_2} - \mathop C\limits^ \bullet {H_2} < C{H_3} - \mathop C\limits^ \bullet H - C{H_3}\]
Lời giải
* Phản ứng khi cho ethylene tác dụng với HBr:
CH2 = CH2 + HBr → CH3 – CH2Br
Cơ chế phản ứng:
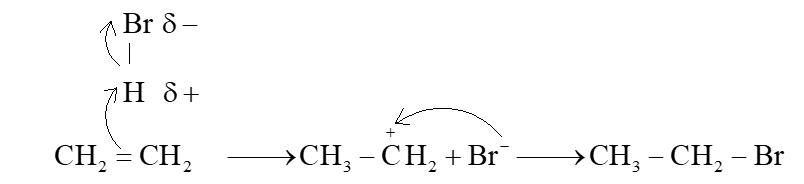
* Phản ứng khi cho ethylene tác dụng với H2O (xúc tác H+):
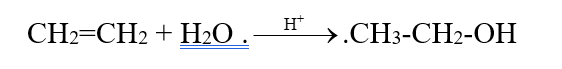
Cơ chế phản ứng:
- Quá trình proton hoá liên kết đôi C = C của ethylene tạo thành carbocation:
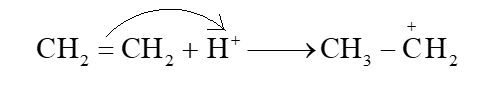
- Quá trình nước cộng hợp vào carbocation:
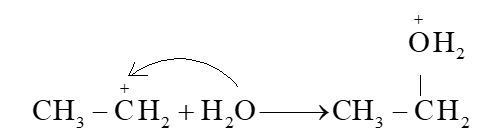
- Quá trình tách proton để tạo alcohol:
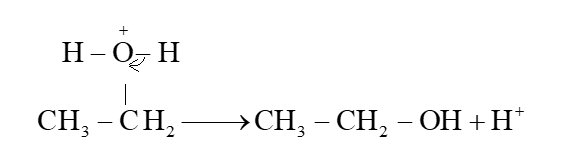
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 9/15 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





















