Bộ 7 Đề thi Học kì 2 Hóa 10 cực hay có đáp án (Đề 7)
29 người thi tuần này 4.7 8.9 K lượt thi 10 câu hỏi 90 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Trắc nghiệm Hóa Ôn tập chương I lớp 10 (có đúng sai, trả lời ngắn - phần 2)
Trắc nghiệm Hóa Ôn tập chương I lớp 10 (có đúng sai, trả lời ngắn - phần 1)
Trắc nghiệm Cấu trúc lớp vỏ electron nguyên tử lớp 10 (có đúng sai, trả lời ngắn)
Trắc nghiệm Cấu trúc lớp vỏ electron nguyên tử lớp 10 (có đáp án - phần 3)
Trắc nghiệm Cấu trúc lớp vỏ electron nguyên tử lớp 10 (có đáp án - phần 2)
Bài tập Cấu trúc lớp vỏ nguyên tử lớp 10 (có lời giải)
Trắc nghiệm Nguyên tố hóa học lớp 10 (có đúng sai, trả lời ngắn)
Bài tập Nguyên tố hóa học lớp 10 (có lời giải)
Danh sách câu hỏi:
Lời giải
1. Viết phương trình phản ứng chứng minh
a. Cl2+ 2NaI → 2NaCl + I2
b. SO2+ Br2+ 2H2O →2HBr + H2SO4
c. 5SO2 + 2KMnO4+ 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
d. S + 3F2SF6
2.Phương trình phản ứng
(1) 2KClO32KCl + 3O2
(2) 2H2S + O2 (thiếu)→ 2S + 2H2O
(3) S + H2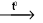 H2S
H2S
(4) H2S + 4Cl2+ 4H2O → H2SO4+ 8HCl
(5) 2Al + 6H2SO4→ Al2(SO4)3+ 3SO2+ 6H2O
(6) Al2(SO4)3+ 3BaCl2⟶ 2AlCl3+ 3BaSO4↓
Lời giải
Hướng dẫn giải
1.
- Đánh số thứ tự từng lọ mất nhãn, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng.
- Sử dụng dung dịch BaCl2
+ Không hiện tượng → HCl
+ Có kết tủa trắng: H2SO4, Na2SO3, AgNO3(nhóm I)
BaCl2+ H2SO4→ BaSO4↓ + 2HCl
BaCl2+ Na2SO3→ BaSO3↓ + 2NaCl
BaCl2+ 2AgNO3→ Ba(NO3)2+ 2AgCl↓
- Lấy HCl vừa nhận ra, cho phản ứng với lần lượt các kết tủa ở trên.
+ Kết tủa tan, có khí thoát ra → kết tủa là BaSO3, chất ban đầu là Na2SO3.
BaSO3+ 2HCl → BaCl2+ SO2↑ + H2O
+ Kết tủa không tan BaSO4; AgCl → nhóm còn lại: H2SO4; AgNO3
- Tiếp tục cho HCl lần lượt vào nhóm còn lại.
+ Có kết tủa trắng → AgNO3.
HCl + AgNO3→ AgCl↓ + HNO3
+ Không hiện tượng → H2SO4.
2.
+ Với dung dịch H2SO4loãng
Fe(OH)2+ H2SO4 → FeSO4+ 2H2O
Fe2O3+ 3H2SO4→ Fe2(SO4)3+ 3H2O
+ Với dung dịch H2SO4đặc, nóng
Cu + 2H2SO4đặc CuSO4 + SO2 + 2H2O
Fe2O3+ 3H2SO4đặc, nóng→ Fe2(SO4)3+ 3H2O
2Fe(OH)2+ 4H2SO4 đặc, nóng→ Fe2(SO4)3 + SO2 + 6H2O
Lời giải
1. a. Với X, Y, Z là các hợp chất của lưu huỳnh:
+ X có tính oxi hóa mạnh và tính axit mạnh ⇒ H2SO4
+ Y là muối trung hòa của kim loại natri ⇒Na2SO3
+ Z là khí không màu, có mùi hắc ⇒SO2
b. Na2SO3+ H2SO4Na2SO4 + SO2 + H2O
c. Khi sục SO2vào dung dịch H2S thì xảy ra hiện tượng là dung dịch bị vẩn đục màu vàng (S). PTHH:
SO2+ 2H2S → 3S↓ + 2H2O
2.
- Thay 13 gam kẽm hạt bằng 13 gam kẽm bột.
- Thực hiện phản ứng ở nhiệt độ thấp hơn (khoảng 20oC).
- Dùng thể tích dung dịch H2SO4gấp ba lượng ban đầu.
a. Ta có
b.
- Thay 13 gam kẽm hạt bằng 13 gam kẽm bột thì tốc độ phản ứng tăng lên do tăng diện tích bề mặt. Kẽm bột phản ứng với axit nhanh hơn kẽm hạt.
- Thực hiện phản ứng ở nhiệt độ thấp hơn (khoảng 20oC) thì tốc độ phản ứng giảm xuống (chậm đi) do giảm nhiệt độ.
- Dùng thể tích dung dịch H2SO4gấp ba lượng ban đầu thì tốc độ phản ứng không thay đổi vì thể tích không ảnh hưởng đến tốc độ phản ứng.
Lời giải
Hướng dẫn giải
⇒ Tạo muối K2SO3và KHSO3
Đặt số mol K2SO3và KHSO3lần lượt là x và y
Theo bài ra ta có hệ phương trình:
mdd saupư= + mKOH = 0,15.64 + 200 = 209,6g
Lời giải
Gọi số mol của Fe, Cu và CuO lần lượt là x (mol), y (mol), z (mol).
Phần 1:
Vì phản ứng tạo ra khí H2nên dung dịch H2SO4 loãng ⇒ Chỉ có Fe và CuO phản ứng. Ta có PTHH
Fe + H2SO4→ FeSO4+ H2
x x x
CuO + H2SO4→ CuSO4+ H2O
y y
Theo phương tình ta có: x + z = 0,1 (1)
Phần 2:
Vì phản ứng tạo khí SO2nên dung dịch H2SO4đặc ⇒ Có Fe, Cu và CuO phản ứng.
Ta có PTHH
2Fe + 6H2SO4→ Fe2(SO4)3+ 3SO2+ 6H2O
x
Cu + 2H2SO4→ CuSO4+ SO2+ 2H2O
y y
CuO + H2SO4→ CuSO4+ H2O
z z
Cô cạn dụng dịch được 26 gam muối khan.
⇒ 200x + 160y + 160z = 26 gam ( 2)
Ta có: 56x + 64y + 80z = 10 gam (3)
Từ (1), (2) và (3) ta có hệ phương trình:
a.
b.
= 0,5 – ( 3.0,05 + 2.0,05 + 0,05) = 0,2 mol
M + 2H2SO4→ MSO4+ SO2+ 2H2O
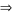 nM= 0,1 mol
nM= 0,1 mol 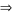 M = = 24
M = = 24 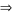 M là Mg
M là Mg
c.
= .0,05 + 0,05 = 0,125 mol
SO2+ Br2+ 2H2O → H2SO4+ 2HBr
0,125 →0,1250,25
2NaOH + H2SO4→ Na2SO4+ 2H2O
NaOH + HBr → NaBr + H2O
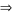 nNaOH= 0,125.2 + 0,25 = 0,5 mol
nNaOH= 0,125.2 + 0,25 = 0,5 mol
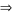 mddNaOH= = 80 gam
mddNaOH= = 80 gam
Lời giải
1.
a. 2Ag + O3 → Ag2O + O2
b. H2S + 4Br2+ 4H2O → H2SO4+ 8HBr
c. SO2 + 2H2S → 2H2O + 3S
d. 2Al + 6H2SO4→ Al2(SO4)3+ 3SO2+ 6H2O
2. Phương trình phản ứng
(1) 4FeS2+ 11O22Fe2O3+ 8SO2
(2) SO2 + 2H2S → 2H2O + 3S
(3) S + H2H2S
(4) 2H2S + 3O2 dư 2H2O + 2SO2
(5) SO2 + Br2+ 2H2O → 2HBr + H2SO4
(6) 2Al + 6H2SO4→ Al2(SO4)3+ 3SO2+ 6H2O
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 4/10 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















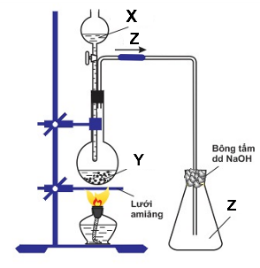 1.Cho sơ đồ thí nghiệm sau:
1.Cho sơ đồ thí nghiệm sau: