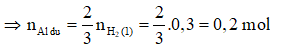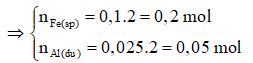Bài tập phản ứng nhiệt nhôm chọn lọc, có đáp án
26 người thi tuần này 4.6 2.4 K lượt thi 15 câu hỏi 60 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 29)
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 28)
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 27)
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 26)
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 25)
Trắc nghiệm tổng hợp Hóa 9 Chương 2: Các loại hợp chất vô cơ có đáp án - Đề 8
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 24)
Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 23)
Danh sách câu hỏi:
Câu 1/15
A. 56,1 gam
B. 61,5 gam
C. 65,1 gam
D. 51,6 gam
Lời giải
Theo định luật bảo toàn khối lượng ta có:
⇔ 8,1 + 48 = 56,1 =
⇒ Chọn A.
Câu 2/15
A. m = 0,27 g
B. m = 2,7g
C. m = 0,54 g
D. m = 1,12 g
Lời giải
2Al + → + 2Fe
2a………a……a…….mol
Theo bài ta có
= 0,58g
⇔ 160a - 102a = 0,58g
⇔ 58a = 0,58
⇔ a = 0,01 mol
⇒ = 2a = 0,02 mol
⇒ = 0,02.27 = 0,54g
⇒ Chọn C.
Câu 3/15
A. Al, Fe, và
B. , Fe và .
C. và Fe
D. Al, Fe và
Lời giải
Theo bài, ta giả sử số mol của là 1 mol, của Al là 3 mol.
8Al + 3→ 4 + 9Fe
Ban đầu 3…………1………........……mol
Ta có vậy Al còn dư sau phản ứng.
Vậy sau phản ứng hỗn hợp gồm có Al dư, , Fe.
⇒ Chọn D.
Câu 4/15
A. 0,3 mol
B. 0,6 mol
C. 0,4 mol
D. 0,25 mol
Lời giải
Vì Y tác dụng với NaOH sinh ra khí nên có Al còn dư → phản ứng hết.
Vậy Y gồm có Al dư, và Fe.
- Y tác dụng với NaOH sinh khí .
- Y tác dụng với HCl sinh khí .
2Al + 6HCl → +3 (2)
Fe + 2HCl → + (3)
⇒ n(2) = = 3/2 . 0,2 = 0,3 mol
⇒ n(3) = = - n(2)
= 0,4 - 0,3 = 0,1 mol
- Phản ứng nhiệt nhôm:
2Al + → + 2Fe (4)
Theo phản ứng (4) ta có:
= 0,2 + 0,1 = 0,3 mol
⇒ Chọn A.
Lời giải
Theo bài ra phản ứng xảy ra hoàn toàn, phần 2 tác dụng với NaOH sinh ra khí Y có Al dư.
Vậy rắn Y gồm , Fe và Al dư.
Xét phần 2:
2Al + 2NaOH + → (1)
0,025 ← 0,0375 mol
Xét phần 1:
2Al + 3 → + (2)
0,025 → 0,0375 mol
Fe + → + (3)
0,1 ← 0,1375 - 0,0375 mol
Phản ứng nhiệt nhôm:
0,2 0,1 ← 0,2 mol
= 0,1.160 + 0,2.27 + 0,05.27 = 22,75g
⇒ Chọn D.
Câu 6/15
A. 45%
B. 50%
C. 71,43%
D. 75%
Lời giải
Phản ứng nhiệt nhôm:
2Al + + 2Fe
Bài toán có hiệu suất phản ứng chưa hoàn toàn.
Vậy hỗn hợp rắn sau phản ứng gồm: Fe, , Al (dư) và (dư)
Chất rắn phản ứng với NaOH có .
Theo định luật bảo toàn khối lượng, ta có:
Xét phản ứng:
Giả sử phản ứng hoàn toàn thì Al sẽ dư
→ Tính hiệu suất phản ứng nhiệt nhôm theo .
⇒ H = = 75%
⇒ Chọn D.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 8/15
A. 5,6 gam
B. 11,2 gam
C. 16 gam
D. 8 gam
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 9/15
A. 33,69%
B. 26,33%
C. 38,30%
D. 19,88%
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10/15
A. Lần lượt NaOH và HCl.
B. Lần lượt là HCl và loãng.
C. Lần lượt NaOH và đặc nóng.
D. Tất a, b, c đều đúng.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11/15
A. Al, Fe, Cu
B. Al, Na, Fe
C. Fe, Cu, Zn
D. Ag, Cu, Fe
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 12/15
A. Dung dịch HCl
B. Nước
C. Dung dịch NaOH
D. Dung dịch
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 13/15
A. Nhôm chỉ có thể khử các oxit kim loại đứng sau H trong dãy hoạt động hóa học.
B. Nhôm chỉ có thể khử các oxit kim loại đứng sau Al trong dãy hoạt động hóa học.
C. Nhôm chỉ có thể khử các oxit kim loại đứng trước và đứng sau Al trong dãy hoạt động hóa học với điều kiện kim loại đó dễ bay hơi.
D. Nhôm khử tất cả các oxit kim loại.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 14/15
A. Fe, Mg, Ag, Al.
B. Cu, Mg, Ag, Al.
C. Fe, Al.
D. Tất cả các kim loại.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 9/15 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.