280 Bài tập Kim loại kiềm, kiềm thổ, nhôm cực hay có lời giải chi tiết (P7)
16 người thi tuần này 4.6 9.8 K lượt thi 16 câu hỏi 50 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 2
Bộ 3 đề thi cuối kì 2 Hóa 12 Chân trời sáng tạo cấu trúc mới có đáp án - Đề 1
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 2
Bộ 3 đề thi cuối kì 2 Hóa 12 Cánh diều cấu trúc mới có đáp án - Đề 1
Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 3
Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 2
Danh sách câu hỏi:
Câu 1/16
A. 0,029.
B. 0,028.
C. 0,026.
D. 0,027.
Lời giải
Đáp án C
quan sát 4 đáp án: a ≤ 0,029 mol → nếu Cu bị đẩy ra hết thì mCu ≤ 0,029 × 64 = 1,856 < 3,72
||→ chứng tỏ Z chứa Cu và Fe (Cu trong dung dịch bị đẩy ra hết). Rõ hơn, quan sát sơ đồ quá trình sau:
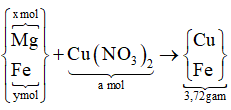
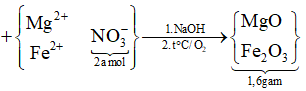
Gọi nMg = x mol và nFe ban đầu = y mol → có ngay 24x + 56y = 3,28 gam.
Trong dung dịch Y bảo toàn điện tích có nFe2+ = (a – x) mol ||→ 1,6 = 40x + 80 × (a – x) ⇄ 80a – 40x = 1,6.
Bảo toàn nguyên tố Fe có trong 3,72 gam gồm a mol Cu và nFe = (x + y – a) mol.
||→ 56 × (x + y – a) + 64a = 3,72 ⇄ 56x + 56y + 8a = 3,72.
Giải hệ 3 ẩn 3 phương trình trên được x ≈ 0,008 mol; y = 0,055 mol và a = 0,024 mol.
||→ theo yêu cầu, đáp án cần chọn là C.
Lời giải
Đáp án C
Quy hỗn hợp thành: Na, Ba và O với số mol lần lượt là a b và c.
+ PT bảo toàn e: a + 2b – 2c = 0,05×2 = 0,1 (1).
+ PT theo số mol H2SO4 đã pứ: a + 2b = 0,19×2 = 0,38 (2).
+ Vì nBaSO4 = 0,12 < nSO42– = 0,19 mol ⇒ ∑nBa = 0,12 mol.
⇒ PT theo số mol Ba là: b = 0,12 (3).
+ Giải hệ (1) (2) và (3) ⇒ nNa = 0,14, nBa = 0,12, nO = 0,14.
⇒ m = 21,9 gam
Câu 3/16
A. 5,54.
B. 5,42.
C. 5,59.
D. 16,61.
Lời giải
Đáp án B
Ta có: nHCl = 0,036 mol, nHNO3 = 0,036 mol, nH2SO4 = 0,024 mol
⇒ ∑nH+ = 0,12 mol || ∑nOH– = 0,08×2×V + 0,23×V = 0,39V.
+ Vì pH = 2 ⇒ Sau pứ trung hòa nH+ dư = 102×(0,36+V) = 0,01V + 0,0036
+ Ta có: ∑nH+ = ∑nOH– + nH+ dư Û 0,12 = 0,39V + 0,01V + 0,0036.
V = 0,291 lít ⇒ nBa(OH)2 = 0,02328 mol.
+ Vì nBa2+ < nSO42– ⇒ m↓ = mBaSO4 = 0,02328×233 ≈ 5,42 gam
Câu 4/16
A. 11,7
B. 15,6
C. 19,5
D. 7,8
Lời giải
Đáp án D
nNaOH = 0,25.2 = 0,5 mol
nAlCl3 = 0,15 mol
PTHH :
3NaOH + AlCl3 → 3NaCl + Al(OH)3
Trước phản ứng : 0,5 mol 0,15 mol
Sau phản ứng : 0,05 mol 0,15 mol
NaOH + Al (OH)3 → NaAlO2 + H2O
Trước phản ứng : 0,05 mol 0,15 mol
Sau phản ứng : 0 0,1 mol
→ m = 0,1 .78 =7,8 g
Câu 5/16
A. K3PO4 và KOH
B. K2HPO4 và K3PO4
C. KH2PO4 và K2HPO4
D. KH2PO4 và H3PO4
Lời giải
Đáp án B
nP2O5 = 0,2 mol
nKOH = 0,45 mol
PTHH : P2O5 + 3H2O →2H3PO4
Vì
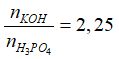
nên phản ứng tạo ra 2 muối K2HPO4 và K3PO4
Lời giải
Đáp án B
Chất không phải chất hữu cơ là Na2CO3
Câu 7/16
A. HCl
B. Ca(OH)2
C. NaNO3
D. NaCl
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 9/16
A. CrO3 tác dụng với dung dịch KOH tạo muối K2CrO4
B. Cr2O3 và Cr(OH)3 đều là chất có tính lưỡng tính
C. Trong môi trường kiềm anion CrO2- bị oxi hóa bởi Cl2 thành anion CrO42-
D. Khi phản ứng với dung dịch H2SO4 loãng nóng kim loại Cr bị khư thành Cr2+
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 15/16
A. Ca, Ba
B. Sr, K
C. Na,Ba
D. Be, Al
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 16/16
A. Al(OH)3.
B. Al2(SO4)3.
C. KNO3.
D. CuCl2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 10/16 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.






















