Đề thi thử tốt nghiệp THPT môn Hóa học Sở GD và ĐT Quảng Bình ( lần 1) có đáp án
132 người thi tuần này 4.6 3.3 K lượt thi 40 câu hỏi 60 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Vĩnh Long có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Gia Lai có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Hà Tĩnh Lần 2 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Đồng Nai lần 2 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT An Giang có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Sơn La lần 3 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Đồng Tháp có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Cần Thơ có đáp án
Danh sách câu hỏi:
Câu 1/40
Lời giải
Đáp án đúng là: C
Trong thực tế, người ta phủ một lớp sơn lên bề mặt sắt, sơn sẽ ngăn cách sắt với môi trường bên ngoài nhờ đó bảo vệ kim loại sắt khỏi bị ăn mòn.
Câu 2/40
Lời giải
Đáp án đúng là: D
Công thức của potassium carbonate là K2CO3.
Câu 3/40
Lời giải
Đáp án đúng là: C
Polypropylene có công thức là (-CH2-CH(CH3)-)n.
Câu 4/40
Lời giải
Đáp án đúng là: D
Mạng tinh thể kim loại không có anion.
Mạng tinh thể kim loại gồm cation kim loại (dao động qua lại quanh vị trí cân bằng) và electron (chuyển động tự do). Khi electron va chạm với cation, nguyên tử kim loại được hình thành, ngay sau đó các nguyên tử này lại tự tách thành cation và electron tự do.
Câu 5/40
Lời giải
Đáp án đúng là: C
Phương pháp Solvay dựa trên độ tan nhỏ của NaHCO3 để thúc đẩy phản ứng:
NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl
Do đó nguyên liệu của phương pháp này không dùng đến NaOH (sodium hydroxide).
Lời giải
Đáp án đúng là: C
Ion Ca2+ (Z = 20) có 20 proton và 18 electron → Tổng 38 hạt 2 loại.
Lời giải
Đáp án đúng là: A
Có 2 tinh dầu hành khách không được phép mang theo lên máy bay là trầm hương và tràm gió.
Câu 8/40
Lời giải
Đáp án đúng là: A
Độ dinh dưỡng các loại phân: (NH4)2SO4 (21,21%); CO(NH2)2 (46,67%); NH4NO3 (35%); NH4Cl (26,17%).
→ (NH4)2SO4 có độ dinh dưỡng thấp nhất.
Câu 9/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 12/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 13/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 14/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 15/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 17/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 18/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 1
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Câu 19: Al2O3 có nhiệt độ nóng chảy rất cao (2050°C) nên việc điện phân nóng chảy Al2O3 nguyên chất sẽ khó thực hiện. Hiện nay, theo công nghệ Hall-Héroult, người ta hoà tan Al2O3 trong cryolite (Na3AlF6) nóng chảy được hỗn hợp chất điện phân có nhiệt độ nóng chảy thấp hơn (khoảng gần 1000°C). Giải pháp này giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp Al lỏng, bảo vệ Al không bị oxi hoá bởi không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới:
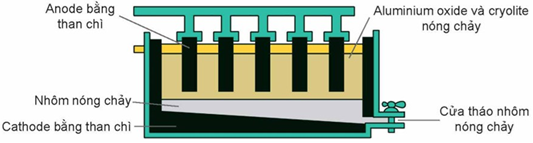
Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế thấp (U = 5 V) và cường độ dòng điện 100 – 300 kA.
Cho biết: Năng lượng điện tiêu thụ theo lí thuyết: ![]() . Trong đó mAl là khối lượng Al được điều chế (gam); F là hằng số Faraday (F = 96485 C/mol); U (V) là hiệu điện thế áp đặt vào hai cực của bình điện phân.
. Trong đó mAl là khối lượng Al được điều chế (gam); F là hằng số Faraday (F = 96485 C/mol); U (V) là hiệu điện thế áp đặt vào hai cực của bình điện phân.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 32/40 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.