Đề thi thử tốt nghiệp THPT môn Hóa Sở GDĐT Yên Bái - Lần 1 năm 2025 có đáp án
79 người thi tuần này 4.6 4.1 K lượt thi 40 câu hỏi 60 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Vĩnh Long có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Gia Lai có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Sơn La lần 3 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Cần Thơ có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Lạng Sơn lần 2 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Tuyên Quang lần 2 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Đà Nẵng lần 1 có đáp án
Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 Sở GD&ĐT Thanh Hóa lần 2 có đáp án
Danh sách câu hỏi:
Câu 1/40
Lời giải
A
Tên gọi của polymer (-CH2-CH=CH-CH2-)n là cao su buna.
Câu 2/40
Lời giải
C
A. Sai, 1,102V là sức điện động chuẩn của pin.
B. Sai, tại cathode: Cu2+ + 2e → Cu
C. Đúng
D. Sai, electron chuyển từ điện cực Zn sang điện cực Cu thông qua dây dẫn điện.
Câu 3/40
Lời giải
C
Phản ứng nhiệt phân polystyrene thuộc loại phản ứng cắt mạch polymer.
Lời giải
B
Có 8 chất lỏng dễ cháy trong bảng trên là: propane; pentane; diethyl ether; hexane; acetaldehyde; ethanol; methanol; trimethylamine.
Lời giải
C
(1) Đúng, baking soda và soda được sản xuất bằng phương pháp Solvay dựa trên các phản ứng chính:
NaCl + NH4HCO3 → NaHCO3↓ + NH4Cl
2NaHCO3 → Na2CO3 + CO2 + H2O
(2) Đúng
(3) Đúng, dầu hỏa không hòa tan O2, H2O và ngăn các chất này tiếp cận Na.
(4) Đúng
Câu 6/40
Lời giải
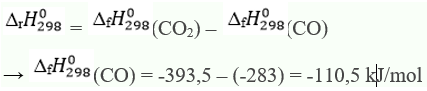
CHỌN A
Câu 7/40
Lời giải
C
Để bảo vệ vỏ tàu biển làm bằng thép (thành phần chính là Fe) người ta thường gắn vào vỏ tàu (phần ngâm dưới nước) những tấm kim loại Zn vì Zn có tính khử mạnh hơn Fe nên Zn là cực âm và bị ăn mòn, Fe là cực dương và được bảo vệ.
Lời giải
A
Trong hợp chất SO3, số oxi hóa của sulfur là +6.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 12/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 13/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 14/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 18/40
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 1
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Nấm men là chất xúc tác cho phản ứng lên men rượu trong điều kiện không có khí oxygen. Quá trình lên men là một quá trình tỏa nhiệt. Từ 250 gam glucose, thực hiện quá trình lên men rượu trong phòng thí nghiệm, kết quả biểu thị theo đồ thị bên.
Kết quả nghiên cứu nhận thấy:
• Tốc độ phản ứng tăng lên và dung dịch trở nên đặc và ấm hơn.
• Từ ngày thứ 10, phản ứng hầu như dừng lại dù trong dung dịch vẫn còn glucose.

Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 32/40 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.























